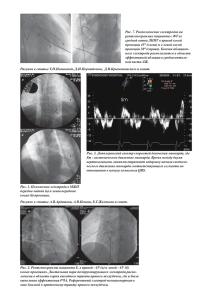
Введение Кардиомиопатия такоцубо – это остро развивающаяся дисфункция миокарда левого желудочка (ЛЖ), впервые описанная в 1990 г. Sato и соавт., характеризующаяся уникальным паттерном регионального, циркулярного снижения сократимости миокарда ЛЖ, приводящим к транзиторному баллонированию ЛЖ во время систолы. В основе заболевания лежит остро развивающаяся гибернация миокарда, зона которой выходит за пределы территории кровоснабжения одной коронарной артерии. Японские авторы обнаружили, что чаще заболевают женщины в период менопаузы. Клиническая картина схожа с таковой при остром инфаркте миокарда с преходящей гипокинезией, акинезией верхушки и средних сегментов левого желудочка (ЛЖ) в сочетании с гиперкинезией базальных отделов, но без стеноза или спазма коронарных артерий при ангиографии. Свое название заболевание получило в честь слова «takotsubo», что в переводе с японского языка означает «горшок для ловли осьминогов». В литературе можно встретить множество синонимов для описания этой патологии, в том числе: синдром такоцубо, синдром «разбитого сердца», стресс-индуцированная кардиомиопатия. Согласно недавнему обзору европейской ассоциации по лечению сердечной недостаточности данная патология была обозначена как «острый, обратимый синдром, сопровождающийся сердечной недостаточностью». В том же обзоре предложено отказаться от термина «кардиомиопатия» в пользу термина «синдром такоцубо» Эпидемиология По данным крупного регистра NIS (the Nationwide Inpatient Sample), опубликованного в 2016 г. и включавшего 6523 пациента с синдромом такоцубо, распространенность заболевания составляет около 2% от всех госпитализаций с подозрением на острый коронарный синдром (ОКС). До 90% пациентов с синдромом такоцубо составляют женщины в постменопаузальном периоде.. По данным Wedekind и соавт. от 2006 г. доля синдрома такоцубо среди женщин, госпитализированных по поводу ОКС, достигает 710%. Причем в большинстве случаев (57,2 %) это азиатские женщины, тогда как европейские составляют лишь 40 % [44]. Однако в другом исследовании большинство больных — мужчины среднего возраста (44±15 лет) ; также описан СТЦ у 83-летнего мужчины . Согласно результатам эпидемиологических исследований, у подавляющего большинства больных с СТЦ (> 76 %) выявлена артериальная гипертензия (АГ), у 57 % — гиперлипидемия, далее — курение (18 %) и сахарный диабет (12 %) Патогенез Патогенез заболевания до конца не изучен, рассматривается несколько возможных теорий: повышенная симпатоадреналовая активность, катехоламининдуцированный множественный коронароспазм, коронарная микроваскулярная дисфункция, прямое кардиотоксическое действие катехоламинов и "катехоламиновое оглушение" (станнирование) миокарда. Частое развитие СТЦ у пациенток потсменопаузального периода объясняют рядом причин. Отмечается, что активность симпатической нервной системы (СНС) у женщин выше, чем у мужчин; более того, у женщин с возрастом она увеличивается . В этой связи можно предполагать некоторые особенности реагирования женщин на стресс: особенности эмоционально-поведенческих реакций, эмоциональная лабильность, повышенная тревожность и раздражительность и пр., особенно у лиц старшей возрастной группы . Известно, что снижение эстрогенной активности во время менопаузы влечет за собой множество изменений. В числе прочих эффектов женские половые гормоны оказывают влияние на СНС (подавляют активность фермента, участвующего в синтезе катехоламинов, увеличивают плотность и функцию 2-адренорецепторов) , метаболизм липидов и липопротеидов (проатерогенное влияние), выраженное кардиопротективное воздействие — 70-80 % обусловленное прямым неметаболическим влиянием на эндотелий сосудов . В условиях дефицита эстрогена происходит рост стимуляции глюкокортикоидов, повышаются уровни норадреналина (НА) в крови и происходит выраженное стресс-индуцированное увеличение концентраций НА , формирующиеся метаболические нарушения, а также изменения в эндотелиальных клетках: повышение уровня гомоцистеина, эндотелина-1, тромбоксана А2, снижение содержания гормона роста и синтеза простациклина ). Гиперсимпатикотония приводит к формированию АГ, развитию и быстрому прогрес-сированию ремоделирования сердечно-сосудистой системы: повышению индекса периферического сопротивлению, снижению сердечного индекса, увеличение толщины стенки ЛЖ ). Таким образом, создается субстрат для развития дисфункции миокарда в виде СТЦ. Исследователи сравнивали сократимость ЛЖ у крыс, перенесших овариэктомию, без эстрогенной заместительной терапии (ЭЗТ): гр. 1, и на ее фоне — гр. 2. Животные подвергались иммобилизационному стрессу (ИС). ИС под общей анестезией ухудшил сократимость ЛЖ в обеих гр., но ЭЗТ предотвращала развитие систолической дисфункции, индуцированной стрессом; артериальное давление (АД) и частота сердечных сокращений (ЧСС) повысились незначительно. Для понимания протективного эффекта эстрогенов были изучены экспрессия c-fos mRNA — маркера клеточной активации и экспрессия mRNA — кардиопротектив-ной субстанции сердца, а также содержание белка теплового шока с молекулярной массой 70 кД и предсердного натрийуретического пептида. Согласно полученных результатов, стресс-индуцированная активность гипоталамо-симпатоадреналовой системы, реализующая действие центральной нервной системы (ЦНС) на органы-мишени, была ниже на фоне эстрогенемии. В исследовании продемонстрировано не только опосредованное через ЦНС, но и прямое кардиопротективное влияние эстрогенов . Это положение может существенно изменить отношение кардиологов к ЭЗТ во время климакса. Согласно одной из гипотез, ключевая роль в патогенезе СТЦ принадлежит повышению уровня катехоламинов (Ктх). Установлено, что в 70-80 % случаев СТЦ связан с чрезмерным продолжительным душевным стрессом и глубокими эмоциональными переживаниями: потеря близкого человека, гнев, раздражение, отчаяние и т. д. . Сообщалось о развитии СТЦ после удара молнии . В 2004г после землетрясения Central Niigata Prefecture японские исследователи в течение 1 мес. наблюдали массовое появление СТЦ, диагностируя заболевание у 16 человек и у 2 ; количество случаев СТЦ после катаклизма возросло в 24 раза . Эмоциональный стресс предшествует внезапному появлению симптомов СТЦ в 26,8 % . У 40 % пациентов с СТЦ триггером для СТЦ также послужил эмоциональный стресс . Одновременно существует предположение, что пагубным для миокарда может оказаться не только сам стресс с гиперсекрецией стрессовых нейромедиаторов (кортизола и адреналина), но и неадекватная поведенческая реакция пациента (например, курение, приводящее к повышению уровня НА и развитию в последующем орга-нопатологии) . Значительная роль в патогенезе СТЦ принадлежит стрессам, ассоциированным с медицинскими манипуляциями — стоматологические процедуры , велоэрго-метрия , холецистэктомия , лечение в палате интенсивной терапии , общее обезболивание , эпидуральная анестезия , интубация трахеи , кардиохирургическое вмешательство и др. Вместе с тем известно, что провоцирующим фактором развития СТЦ могут послужить и другие причины: физический стресс — до 37,8 % , массивная травма , инсульты, субарахноидальные кровоизлияния, черепно-мозговые травмы, феохромоцитома и пр. Факторы, предрасполагающие к развитию СТЦ, весьма разнообразны и могут включать неотложные медицинские состояния: субарахноидальное кровоизлияние лобэктомию, менингит и эпидуральный абсцесс шейного отдела спинного мозга, терминальную хроническую почечную недостаточность , острое нарушение мозгового кровообращения , эндокраниальное оперативное вмешательство и эпилептический статус , задний лейкоэнцефалопатический синдром , амиотрофический латеральный склероз , отравление окисью углерода , синдром отказа от алкоголя и наркотических препаратов . Описаны случаи развития СТЦ, индуцированной приемом нестероидных противовоспалительных препаратов — локсопрофен , люмиракоксиб (ингибитор циклооксигеназы-2) , отмены наркотического анальгетика бупренорфина у детей , а также антибиотика левофлоксацина . В ряде случаев причины заболевания могут быть вовсе не выявлены ; отсутствие какихлибо известных предшествующих провоцирующих факторов не исключает возможности развития заболевания. Независимо от природы стрессорных факторов, их влияние на организм реализуется совокупностью метаболических и нейроэндокринных изменений, активированием симпатоадреналовой системы и повышением плазменного уровня Ктх. Гипотеза, рассматривающая симпатическую гиперактивацию в качестве первопричины формирования СТЦ, подтверждена рядом исследований. Установлено, что заболевание может быть спровоцировано чрезмерной симпатической стимуляцией а содержание НА в плазме крови повышено у подавляющего большинства пациентов с СТЦ (74,3 %) . Плазменный уровень НА может превышать нормативные показатели в 3 раза (в среднем 0,98 мкг/л, при норме 0,3 мкг/л). Формирование своеобразной систолической дисфункции миокарда при СТЦ объясняют следующим образом. Предполагают, что клеточные механизмы поражения миокарда при СТЦ отличаются от таковых при эпизодах преходящей ишемии, вызванных стенозом КА. Согласно гипотезе, при изучаемом синдроме высокий уровень циркулирующего адреналина запускает механизм внутриклеточного сигнального движения в кардиомио- цитах (КМЦ) желудочков, от G ^)-протеинов к G (^-протеинам, сигнализируя через р2адренорецептор. Несмотря на этот сигнал, G (^-протеин р2-адренорецепторов защищает от проапоптозного эффекта гиперактивации Р'-адренорецепторов, что и характеризуется отрицательным инотропным эффектом. Последний более выражен в миокарде верхушки, где плотность Р-адренорецепторов выше ; именно с этим, по мнению исследователей, и связано развитие гипокинеза верхушки ЛЖ при гипер-контрактильности базальных отделов, присущие СТЦ. Диагностические критерии В течение последних 10 лет представления о диагностике синдрома такоцубо меняются от диагноза-исключения (зона гипокинезии в области верхушки в сочетании с интактными коронарными артериями по данным коронарной ангиографии) к пониманию того. что синдром такоцубо является самостоятельным заболеванием и имеет специфические признаки:гибернация миокарда, признаки воспаления и отека миокарда, что может быть подтверждено при проведении магнитной резонансной томографии (МРТ) миокарда в Т2 режиме (наиболее характерным МРТ признаком является усиление Т2 сигнала и трансмуральное распределение в области снижения локальной сократимости). В настоящее время не существует общепринятых диагностических критериев для постановки диагноза «синдром такоцубо». В мировой литературе предложено несколько вариантов критериев, основанных на локальных регистрах. Наиболее распространенными на сегодняшний день являются модифицированные критерии Mayo (2011 г., США, Европа), согласно которой синдром такоцубо – острое кардиологическое событие, обычно сопровождающееся болью за грудиной и/или одышкой. Общим среди всех вариантов является наличие транзиторного нарушения локальной сократимости левого желудочка, зона которой выходит за пределы территории кровоснабжения одной коронарной артерии, несоответствие уровня повышения маркеров повреждения миокарда объему повреждения сердечной мышцы и отсутствие признаков атеротромбоза и признаков острого повреждения атеросклеротической бляшки по данным коронарной ангиографии.Часто в анамнезе отмечается триггерный стрессовый момент, хотя он не всегда присутствует; отсутствие фе-охромоцитомы, миокардита. Формы синдрома такоцубо Нарушение локальной сократимости ЛЖ является обратимым. Обычно систолическая функция полностью восстанавливается в течение 10-14 дней. Наиболее известной является типичная, «апикальная» форма синдрома такоцубо, при которой развивается циркулярное баллонирование всех верхушечных сегментов ЛЖ. Однако описаны также и «неапикальные» формы синдрома такоцубо, распространенность которых, по данным локальных регистров, варьирует от 8,3% до 40%. На сегодняшний день выделяют следующие атипичные формы синдрома такоцубо: • средневентрикулярная форма (средне-верхушечные, средние, средне-базальные и базальные сегменты) – до 20% случаев; • базальная форма (нижне-базальные и боковые сегменты) – до 3% случаев; • инвертированная форма (циркулярное вовлечение базальных сегментов с гиперкинезией верхушечных сегментов) – до 5%; • фокальная форма (локальное нарушение сократимости с признаками баллонирования). Правомерность выделения фокальной формы синдрома такоцубо по-прежнему вызывает множество споров. Дифференциальная диагностика с очаговыми формами миокардита и инфарктом миокарда предполагает обязательное проведение МРТ сердца и проведения интракоронарного ультразвука у этой категории пациентов. В литературе также встречаются описания синдрома такоцубо с изолированным вовлечением правых отделов сердца. Клиническая картина Клиническая картина острой фазы синдрома такоцубо зачастую неотличима от симптомов острого коронарного синдрома с подъемом или без подъема. сегмента ST. По данным международного регистра такоцубо (Taco-registry) самыми частыми симптомами заболевания являются: боль за грудиной, одышка и синкопе. Реже заболевание манифестирует с признаков острой сердечной недостаточности, остановки кровообращения на фоне жизнеугрожающих нарушений ритма, острой митральной недостаточности. При аускультации сердца может выслушиваться грубый систолический шум в проекции аорты, что требует исключения острой обструкции выносящего тракта ЛЖ. Одним из основных, хотя и необязательных, критериев постановки диагноза синдрома такоцубо является наличие стрессового фактора, приводящего к развитию заболевания. Первые описания синдрома такоцубо были опубликованы после землетрясения в Японии, и в течение длительного времени считалось, что только эмоциональные триггеры могут быть причиной синдрома такоцубо, однако результаты недавних исследований демонстрируют, что физические факторы приводят к развитию синдрома такоцубо даже чаще, чем психо-эмоциональные (табл. 2). На сегодняшний день исследователями синдрома такоцубо предложена новая классификация заболевания. В связи с большим количеством физических факторов, которые могут приводить к развитию острого баллонирования участков миокарда, что предположительно является единой патофизиологической реакцией сердечно-сосудистой системы на стресс, предложено определить все варианты синдрома такоцубо, развившегося под воздействием физических факторов (хирургическая травма, лекарственное воздействие, сепсис, кровопотеря и т.д.), как вторичный синдром такоцубо, тогда как классическое развитие заболевания под воздействием психо-эмоционального стресса решено обозначить как первичный синдром такоцубо. Учитывая сходство клинической картины с таковой при инфаркте миокарда, исходно пациенты с кардиомиопатией Такоцубо, как правило, проходят всестороннее кардиологическое обследование. При данной патологии в большинстве случаев выявляются электрокардиографические отклонения. Обычно наблюдается подъем сегмента ST, наиболее часто в передних отведениях. Также может выявляться инверсия зубца T, удлинение интервала QT (QTc), а также патологический зубец Q. Также характерно повышение уровня сердечных биомаркеров, включая тро-понины и креатинкиназу. Однако, в отличие от динамики повышения уровней сердечных биомаркеров при остром инфаркте миокарда, интенсивность повышения уровней лабораторных маркеров при кардиомиопатии Такоцубо, как правило, менее выражена. В исследовании, проведенном Sharkey и соавт. у 59 пациентов с кардиомиопатией Такоцубо, пиковый уровень тропонина T был ниже (0,64+0,86 нг/мл), чем при остром инфаркте миокарда (3,88+4,9 нг/мл) . По данным коронароангиографии не выявляется окклюзий коронарных артерий, которые бы соответствовали степени выраженности и зонам дисфункции левого желудочка. Однако, учитывая пожилой возраст многих пациентов, зачастую отмечается одновременное наличие кардиомиопатии Такоцубо и небольшой ишемической болезни сердца (ИБС). Трансторакальная эхокардиография и левая вентри-кулография являются определяющими методами диагностики кардиомиопатии Такоцубо. В последнее время для оценки функции сердца также стала использоваться магнитно-резонансная томография (МРТ) сердца. В частности, в отличие от острого инфаркта миокарда, для данной патологии характерно отсутствие позднего гадолини-евого усиления (по данным МРТ) . Кроме того, может наблюдаться миокардиальный отек, однако это неспецифичный признак кардиомиопатии Такоцубо, так как он также может выявляться при миокардитах или остром инфаркте миокарда . При инфаркте миокарда, как правило, наблюдается локальное снижение сократимости миокарда, а для кардиомиопатии Такоцубо характерна гипокинезия или дискинезия апикальных сегментов миокарда на фоне относительно сохранного функционирования остальной части левого желудочка. Лечение и прогноз Несмотря на выраженную клиническую картину при кардиомиопатии Такоцубо, данное состояние является транзиторным и обычно разрешается без инвазивных вмешательств. При наличии кардиогенного шока и нестабильности гемодинамических показателей для обеспечения кратковременной поддержки пациента могут потребоваться более агрессивные и инвазивные методы терапии. В острый период заболевания необходимо проведение непрерывного мониторирования основных показателей функции сердца, что связано с риском желудочковых аритмий. Использование имплантируемых дефибрилляторов не показано в острый период заболевания из-за обратимости данного состояния. Однако в ходе выполнения последующих исследований необходимо оценить плюсы от использования переносных кардиовертеров-дефибрилляторов в острый период заболевания у пациентов с систолической дисфункцией левого желудочка до момента выздоровления . Учитывая удлинение интервала QT, ассоциированное с кардиомиопатией Такоцубо, аритмия типа «torsades de pointes» также может быть потенциальным вариантом осложнения данного заболевания . Поэтому необходимо проводить тщательный мониторинг уровня электролитов и восполнять их при необходимости. Препараты, удлиняющие интервал QT должны использоваться только при наличии четких клинических показаний. Медикаментозная терапия на начальном этапе лечения кардиомиопатии Такоцубо обычно включает стандартную терапию, используемую при систолической сердечной недостаточности, а именно: ингибиторы ангиотензин-превращающего фермента (АПФ), диуретики и бета-блокаторы . При наличии сопутствующего легкого или умеренного атеросклероза также часто назначается аспирин . Четких рекомендаций относительно длительности лечения нет. Учитывая то, что кардиомиопатия Такоцубо является транзиторным состоянием, обычно эти препараты длительно не назначаются (при отсутствии других показаний). Длительность лечения составляет 1-4 нед, у большинства пациентов в течение этого периода наблюдается восстановление функции сердца. Из-за риска рецидива некоторые врачи предпочитают назначать бета-блокаторы на длительный срок для вторичной профилактики, однако этот подход остается противоречивым. По данным Elesber и соавт., средняя ежегодная частота рецидива кардиомиопатии Такоцубо в течение первых нескольких лет составляет 2,9%. И, несмотря на то что многим пациентам назначались бета-блокаторы, авторы не выявили статистически значимых отличий по- казателей профилактики рецидива заболевания по сравнению с группой контроля. Однако следует учитывать небольшую выборку исследования . Так, прием ингибиторов АПФ и блокаторов ангиотензиновых рецепторов с более высокой вероятностью, чем бетаблокаторы, снижал риск развития рецидива . При более тяжелом состоянии с нестабильностью гемодинамических показателей и рефрактерностью к инфузионной терапии или ее непереносимостью у пациентов без обструкции ВТЛЖ возможна инотропная поддержка (добутамин и дофамин). Однако при наличии обструкции ВТЛЖ препараты с положительным инотропным и хронотропным эффектами могут усугубить обструкцию выносящего тракта и привести к снижению сердечного выброса, особенно на фоне повышенного уровня катехоламинов. В то же время использование бета-блокаторов при обструкции ВТЛЖ позволяет снизить частоту сердечных сокращений, улучшить кровенаполнение желудочков и может привести к разрешению гемодинамической нестабильности. Несмотря на частое назначение (с целью поддержания гемодинамики пациентам с кардиогенным шоком) внутриаортальной баллонной контрпульсации, она может отрицательно повлиять на сердечный выброс при кардиомиопатии Такоцубо с обструкцией ВТЛЖ за счет снижения постнагрузки . В случае гипотонии, требующей вазопрессорной поддержки, следует отдать предпочтение агонистам альфа-адренергических рецепторов, таким как фенилэфрин (мезатон), так как они обладают минимальным инотропным эффектом и с гораздо меньшей вероятностью усиливают обструкцию выносящего тракта . Учитывая риск тромбоэмболии на фоне стаза крови в сердце при тяжелой систолической дисфункции, исходя из данных, полученных в отношении острого инфаркта миокарда, необходимо рассмотреть вопрос о назначении антикоагулянтов. По данным Tsuchihashi и соавт., в число распространенных внутрибольничных осложнений входят: отек легких (22 %), кардиогенный шок (15%) и желудочковые аритмии (9%) . Аритмии являются распространенным осложнением, выявляемым примерно у 1/4 пациентов с кардиомиопатией Такоцубо; наиболее частый вид нарушения ритма сердца является фибрилляция предсердий (7%). При этом у мужчин с большей вероятностью, чем у женщин, развиваются угрожающие жизни желудочковые тахиаритмии (по сравнению с фибрилляцией или трепетанием предсердий у женщин) . Учитывая транзиторный характер кардиомиопатии Такоцубо, в целом прогноз благоприятный. Описаны случаи пер-систирующего апикального баллонирования, однако оно выявляется у малого количества пациентов [55, 56]. Уровень внутрибольничной летальности от кардиомиопатии Такоцубо не превышает 8%, при этом медиана длительности госпитализации составляет 4 дня, а 4-летняя частота рецидива - 11,4%. У подавляющего большинства выживших пациентов наблюдается восстановление функции желудочков сердца в течение 1-4 нед. Заключение В данный момент синдром Такоцубо является весьма популярной и интересной темой для обсуждения, так как является не до конца изученной. синдром Такоцубо - заболевание, характеризующееся стресс-индуцированной локализованной дисфункцией сердца. Своевременное выявление и дифференциальная диагностика с острым коронарным синдромом очень важны в плане оптимизации терапии. Обычно развитию кардиомиопатии предшествует физический или эмоциональный стрессовый фактор. Однако провоцирующий фактор не всегда удается выявить. Лечение в большинстве случаев включает консервативную и поддерживающую терапию. Агрессивная тактика лечения проводится при возникновении острых и тяжелых осложнений, таких как гипотензия, желудочковые аритмии и тромбоэмболия. Прогноз у большинства пациентов, переживших первоначальный острый период заболевания, очень хороший. Восстановление функции левого желудочка, как правило, наблюдается в течение нескольких недель