Основные типы кристаллических решёток
реклама
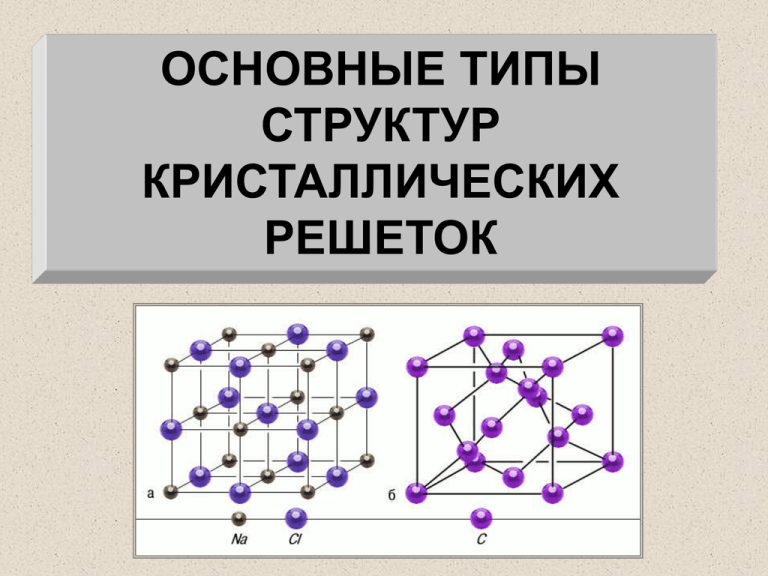
ОСНОВНЫЕ ТИПЫ СТРУКТУР КРИСТАЛЛИЧЕСКИХ РЕШЕТОК АГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВА ВСЕ ВЕЩЕСТВА СОСТОЯТ ИЗ ЧАСТИЦ МОЛЕКУЛ ИОНОВ АТОМОВ Кристаллическая решетка – это пространственный каркас, в котором все частицы обозначены в виде точек. Точки соединены прямыми линиями Узлы решетки ТИПЫ КРИСТАЛЛИЧЕСКИХ РЕШЕОК ИОННЫЕ АТОМНЫЕ МОЛЕКУЛЯРНЫЕ МЕТАЛЛИЧЕСКИЕ ИОННЫЕ РЕШЕТКИ Строение: -- в узлах расположены ионы ( К+ и А- ) -- между частицами существует ионная связь Особенности: --нельзя выделить отдельные молекулы; -- характерны для солей, оксидов и гидроксидов металлов; -- вещества твердые и прочные; -- tплав веществ высокие; -- растворимы в воде. АТОМНЫЕ РЕШЕТКИ Строение: -- в узлах находятся отдельные атомы; -- частицы связаны прочными ковалентными связями. Атомная кристаллическая решетка алмаза Особенности: -- невозможно выделить отдельные молекулы; -- решетки характерны для карбидов и силицидов: песка, кварца; -- вещества имеют высокие tплав ( у кварца – 3500 0С) , практически нерастворимы. Кристаллическая решетка оксида кремния –SiO2 Портретный алмаз Алмаз «Горняк» Алмаз «Шах» Кварц МОЛЕКУЛЯРНЫЕ РЕШЕТКИ Строение: в узлах находятся отдельные молекулы с ковалентной неполярной связью, между ними действуют слабые межмолекулярные силы ( N2, O3 ) с ковалентной полярной связью, между ними действуют слабые межмолекулярные силы (HCl, H2O) Кристаллическая решетка иода Особенности: -- такие решетки характерны для льда, твердых простых веществ, благордных газов, Н2, О2, N2. I2, «сухого льда», Р4,S8,сахара; -- вещества имеют низкие tплав, нетвердые, летучие. МЕТАЛЛИЧЕСКИЕ КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ В узлах находятся ион-атомы, которые связываются обобществленными электронами, передвигающимися между ними в различных направлениях ГРАНЕЦЕНТРИРОВАННАЯ ГЕКСАГОНАЛЬНАЯ Na, K, Ba, Cr, Fe Al, Ca, Ni, Cu, Ag, Au Mg, Ti, Co, Zn, Cd ОБЪЕМНОЦЕНТРИРОВАННАЯ Положение элементов в Периодической системе Д.И.Менделеева и типы кристаллических решеток их простых веществ











