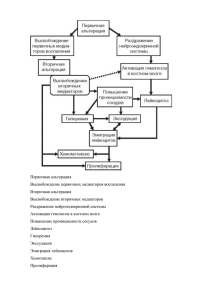
Воспаление – комплексная защитная стромально-сосудистая реакция организма в ответ на действие патологического фактора. Воспаление (inflammatio, от лат. in-flammare - воспламенять) сформировавшаяся в процессе эволюции реакция организма на местное повреждение, характеризующаяся явлениями альтерации, расстройств микроциркуляции (с экссудацией и эмиграцией) и пролиферации, направленными на локализацию, уничтожение и удаление повреждающего агента. По этиологии различают 2 группы воспалений: Специфическим является воспаление, которое вызывается определенными причинами (возбудителями). Это воспаление, вызываемое микобактериями туберкулеза, воспаление при лепре (проказе), сифилисе, актиномикозе. Воспаления, вызываемые другими биологическими факторами (кишечная палочка, кокки), физическими, химическими факторами, относятся к банальным воспалениям. По времени протекания воспаления выделяют: 1) острое – протекает 7—10 дней; 2) хроническое – развивается от 6 месяцев и более; 3) подострое воспаление – по продолжительности находится между острым и хроническим. По морфологии (патологоанатомическая классификация) различают экссудативное и пролиферативное (продуктивное) воспаление. Причины воспаления могут быть химическими, физическими и биологическими. Среди биологических факторов наибольшее значение имеют вирусы, бактерии, грибы и животные паразиты. К биологическим причинам воспаления могут быть отнесены циркулирующие в крови антитела и иммунные комплексы, которые состоят из антигена, антител и компонентов комплемента, причем антиген может быть немикробной природы. К физическим факторам, вызывающим воспаление, относят лучевую и электрическую энергию, высокие и низкие температуры, различного рода травмы. Химическими факторами воспаления могут быть различные химические вещества, токсины и яды. Поскольку наиболее частой причиной воспаления являются инфекционные агенты, его делят по этиологии на инфекционное (септическое) и неинфекционное (асептическое). ПАТОГЕНЕЗ ВОСПАЛЕНИЯ Любое воспаление включает 3 основных компонента: • альтерацию - повреждение клеток и тканей; • расстройство микроциркуляции с экссудацией и эмиграцией; • пролиферацию - размножение клеток и восстановление целостности ткани. Соответственно различают: альтеративное воспаление, экссудативное воспаление, пролиферативное (продуктивное) воспаление и - как его отдельный вариант - гранулематозное воспаление. Патогенез воспаления представляет собой сложное сочетание нервных, гуморальных и эффекторных механизмов, лежащих в основе большого числа воспалительных феноменов, составляющих вышеперечисленные явления. 2. Альтерация (alteratio, от лат. alterare - изменять), или дистрофия, повреждение ткани, нарушение в ней питания (трофики) и обмена веществ, ее структуры и функции. Различают первичную и вторичную альтерацию. Зона первичной альтерации Причина формирования первичной альтерации: флогогенный фактор, действующий на ткань. Локализация первичной альтерации: место прямого контакта причины воспаления с тканью (эта зона — эпицентр очага воспаления). Основные механизмы первичной альтерации • Повреждение мембранных структур и внутриклеточных ферментов, а также структур межклеточного вещества. • Расстройства энергетического обеспечения функций и пластических процессов в повреждённой ткани. • Нарушения трансмембранного переноса и градиента ионов, соотношения их между собой, содержания жидкости внутри и за пределами клетки и в зоне альтерации в целом. Проявления первичной альтерации • Расстройства функции повреждённых, но ещё жизнеспособных участков ткани вне зоны некроза. • Некроз. • Значительные физико-химические изменения. • Различные формы дистрофии. Время начала развития вышеуказанных изменений колеблется в широком диапазоне и определяется особенностями флогогенного фактора, ткани или органа, подвергшегося его воздействию, реактивности организма. Тем не менее первые изменения выявляются сразу после воздействия причины воспаления на ткань. Зона вторичной альтерации Причины вторичной альтерации • Эффекты флогогенного агента (хотя за пределами эпицентра очага воспаления эффективность его патогенного воздействия значительно ниже). • Влияние факторов, вторично формирующихся в зоне первичной альтерации в связи с образованием медиаторов воспаления, развитием метаболических, физико-химических и дистрофических изменений. Локализация вторичной альтерации • Частично в месте контакта флогогенного агента с тканью (там, где сила его воздействия была минимальной). • В основном вокруг области первичной альтерации. Обычно площадь этой зоны значительно больше площади первичной. Механизмы развития вторичной альтерации • Расстройства местных механизмов нервной регуляции в связи с повреждением тел нейронов, нервных стволов и/или их окончаний, синтеза, накопления и высвобождения из них нейромедиаторов. • Нарушение выброса нейромедиаторов (норадреналина, ацетилхолина и др.) из нервных терминалей симпатической и парасимпатической системы в очаге воспаления и стадийные изменения чувствительности тканей к нейромедиаторам в этом очаге. • Расстройства аксонного транспорта трофических и пластических факторов (углеводов, липидов, белков, адениннуклеотидов, нуклеиновых кислот, БАВ, ионов и других агентов) от тел нейронов к соматическим клеткам. • Стадийные изменения тонуса сосудов микроциркуляторного русла и в связи с этим — расстройства кровообращения • БАВ, поступающие в зону вторичной альтерации из зоны первичной альтерации, а также образующие за пределами очага воспаления. В совокупности эти изменения обусловливают расстройства обмена веществ, значительные физико-химические сдвиги в зоне вторичной альтерации, развитие различных видов дистрофий и даже некроза. Проявления вторичной альтерации • Изменения структуры клеток и межклеточного вещества тканей, обычно обратимые (например, признаки повреждения клеток, архитектуры ткани и др.). • Расстройства метаболизма (выражается различными отклонениями в обмене веществ и развитии). • Умеренные отклонения физико-химических параметров (например, рН, осмоляльности жидкости, температуры тканей, трансмембранного распределения ионов). • Обратимые изменения функции тканей и органов. Время начала формирования вторичной альтерации. Как следует из характеристики механизмов развития изменений в зоне вторичной альтерации, её формирование несколько сдвинуто во времени (секунды—минуты) по сравнению со сроками формирования зоны первичной альтерации. Интенсивность формирования различных зон альтерации, выраженность изменений в них и соотношение их размеров существенно различаются и в каждом конкретном случае зависят от причины воспаления, структурных и функциональных особенностей ткани или органа, в котором развивается воспаление, реактивности организма и других условий. Далее анализируется спектр изменений (морфология, метаболизм, медиаторы воспаления, изменения физико-химические и функциональные) в очаге воспаления. Механизмы, проявления и последствия этих изменений рассмотрены в основном для зоны вторичной альтерации. Это объясняется тем, что при большинстве форм воспаления именно эта зона доминирует как по занимаемой ею площади, так и по своему значению. Именно в этой зоне формируются и реализуются процессы, обеспечивающие локализацию, нейтрализацию, уничтожение и элиминацию флогогенного агента, а также ликвидацию последствий его патогенного воздействия. 4.Стадии расстройства микроциркуляции: 1. Кратковременный спазм артериол:результат рефлекторного возбуждения вазоконстрикторов на воздействие флогогена (несколько сек–мин). 2. Артериальная гиперемия:увеличение притока артериальной крови и кровенаполнения ткани. Способствует усилению оксигенации тканей, снижению степени ацидоза, активации обмена веществ. 3. Венозная гиперемия:сопровождается замедлением тока крови, расширением просвета посткапилляров и венул. В механизме выделяют 3 группы факторов: нарушения реологических свойств крови; изменения сосудистой стенки; тканевые изменения. 4. Предстаз:периодические маятникообразные движения крови «вперёд ↔ назад» в результате механического препятствия оттоку крови по посткапиллярам, венулам и венам агрегатами форменных элементов крови в просвете сосуда и пристеночными микротромбами. 5. Стаз:возникает в результате закрытия просвета микрососудов агрегатами клеток изнутри и сдавления экссудатом снаружи. Является завершающей стадией сосудистых изменений. 3. В ходе первичной и вторичной альтерации высвобождаются большие количества разнообразных медиаторов и модуляторов воспаления 5. Экссудация — компонент воспаления, включающий в себя триаду: сосудистые реакции и изменения кровообращения в очаге воспаления; выход жидкой части крови из сосуда (собственно экссудацию); эмиграцию (выход лейкоцитов в очаг воспаления и развитие фагоцитарной реакции). Основная причинаэкссудации — увеличение проницаемости стенок микрососудов вследствие множества процессов, повреждающих их стенку. Основные факторы механизма экссудации: 1) повышение проницаемости сосудов (венул и капилляров) в результате воздействия медиаторов воспаления и в ряде случаев самого воспалительного агента — ведущий фактор; 2) увеличение кровяного (фильтрационного) давления в сосудах очага воспаления вследствие гиперемии; 3) возрастание осмотического и онкотического давления в воспаленной ткани в результате альтерации и начавшейся экссудации и, возможно, снижение онкотического давления крови из-за потери белков при обильной экссудации. Виды экссудата 1. Серозный экссудат: состоит из полупрозрачной жидкости, богатой белком (до 2–3%), и немногочисленных клеток, в том числе форменных элементов крови (ФЭК). 2. Фибринозный экссудат: содержит большое количество фибриногена и фибрина. 3. Гнойный экссудат:мутная густая жидкость, содержащая до 6–8% белка и большое количество различных форм лейкоцитов, микроорганизмов, погибших клеток повреждённой ткани. 4. Геморрагический экссудат:содержит большое количество белка и эритроцитов, а также другие ФЭК. 5. Гнилостный (ихорозный) экссудат: любой вид экссудата может приобрести гнилостный (ихорозный) характер при внедрении в очаг воспаления гнилостной микрофлоры (анаэробы). 6. Смешанные формыэкссудата могут быть самыми разнообразными (например, серознофибринозный, гнойно-фибринозный, гнойно-геморрагический и др.). Значение процесса экссудации в очаге воспаления Адаптивное: транспорт медиаторов воспаления доставка иммуноглобулинов в очаг воспаления удаление из крови метаболитов и токсинов задержка и/или фиксация в очаге воспаления флогогена и продуктов его действия на ткань Патогенное: сдавление, смещение органов и тканей экссудатом возможность излияния экссудата в полости тела и сосуды формирование абсцессов, развитие флегмон 7.Эмиграция (emigratio, от лат.emigrare — выселяться, переселяться) — выход лейкоцитов из сосудов в ткань. Осуществляется путем диапедеза через стенку венул и является ключевым событием патогенеза воспаления. Стадии процесса эмиграции лейкоцитов в очаге воспаления: 1. краевое стояние лейкоцитов; 2. адгезия к эндотелию и проникновения через сосудистую стенку; 3. направленное движение лейкоцитов в очаге воспаления. На стадии краевого стояния(маргинации) условно выделено четыре последовательных этапа. В стадии адгезии и выхода лейкоцитов выделяют 2 этапа: устойчивой («плотной») адгезии (1) и прохождения лейкоцитов через стенку микрососуда (2). Значение эмиграции лейкоцитов в очаг воспаления: поглощение и деструкция флогогенного фактора; поглощение и деструкция поврежденных клеток и неклеточных структур; синтез и выделение медиаторов воспаления; поглощение и «процессинг» антигенов и презентация последних лимфоцитам; развитие иммунных и/или аллергических реакций. 8.Под воспалительной пролиферацией (proliferate, от лат. proles - потомство, ferre - создавать) понимают размножение местных клеточных элементов в очаге воспаления. Пролиферация развивается с самого начала воспаления наряду с явлениями альтерации и экссудации, но становится преобладающей в более поздний период процесса, по мере стихания экссудативно-инфильтративных явлений. Первоначально она в большей мере выражена на периферии очага. Важнейшим условием прогрессирования пролиферации является эффективность очищения очага воспаления от микроорганизмов или другого вредного агента, продуктов альтерации тканей, погибших лейкоцитов (раневое очищение). Ведущая роль в этом отводится макрофагам - гематогенного (моноциты) и тканевого (гистиоциты) происхождения. Раневое очищение происходит путем внеклеточной деградации поврежденной ткани и фагоцитоза. Оно осуществляется под регуляторным влиянием цитокинов с помощью таких ферментов, как протеогликаназа, коллагеназа, желатиназа. Активация этих ферментов может происходить под воздействием активатора плазминогена, высвобождаемого при участии цитокинов из мезенхимальных клеток. Простагландины, высвобождаясь вместе с ферментами, могут, со своей стороны, индуцировать протеиназы и вносить свой вклад в процессы деградации. Фагоцитоз был открыт и понят как важнейший элемент воспаления и естественного иммунитета И.И. Мечниковым в 1882 г. И.И. Мечников выделил 4 фазы фагоцитоза: 1) фаза приближения: выход лейкоцита из сосуда и приближение к объекту фагоцитоза под действием хематтрактантов; 2) фаза прилипания (контактная); 3) фаза погружения: обволакивание и погружение объекта внутрь фагоцита; образуется особая вакуоль, где скапливаются лизосомы; 4) фаза переваривания, результатом которой могут быть 2 варианта исхода: а) адекватное дозированное освобождение лизосомальных ферментов, разрушающее только флогоген (сам фагоцит остается интактным); б) чрезмерное выделение лизосомальных ферментов, что ведет к разрушению объекта фагоцитоза и самого фагоцита. Пролиферация осуществляется главным образом за счет мезенхимальных элементов стромы, а также элементов паренхимы органов. В ней участвуют камбиальные, адвентициальные, эндотелиальные клетки. В результате дифференцировки стволовых клеток соединительной ткани - полибластов - в очаге появляются эпителиоидные клетки, фибробласты и фиброциты. Основными клеточными элементами, ответственными за репаративные процессы в очаге воспаления, являются фибробласты. Они продуцируют основное межклеточное вещество - гликозаминогликаны, а также синтезируют и секретируют волокнистые структуры - коллаген, эластин, ретикулин. В свою очередь, коллаген является главным компонентом рубцовой ткани. Регуляция пролиферации. Процесс пролиферации находится под сложным гуморальным контролем. Решающее значение здесь имеют макрофаги - основные источники фактора роста фибробластов - термолабильного белка, стимулирующего пролиферацию фибробластов и синтез коллагена - усиливают привлечение фибробластов в очаг воспаления, секретируя IL-1 и фибронектин. -стимулируют пролиферацию эндотелиальных и гладкомышечных клеток сосудистой стенки, базальной мембраны и, таким образом, образование микрососудов. Угнетение или стимуляция системы мононуклеарных фагоцитов соответственно ослабляет или усиливает развитие грануляционной ткани в очаге гнойного воспаления. В свою очередь, макрофаги опосредуют регуляторное влияние на фибробласты и пролиферацию Тлимфоцитов. Последние же активируются протеиназами, образующимися в очаге воспаления в результате распада ткани. Протеиназы могут оказывать непосредственное влияние как на макрофаги, так и на фибробласты. Макрофаги и лимфоциты могут высвобождать моно- и лимфокины, не только стимулирующие, но и угнетающие фибробласты, выступая в качестве истинных регуляторов их функций. Фибробласты зависят также от тромбоцитарного фактора роста, являющегося термостабильным белком с высоким содержанием цистеина и молекулярной массой 30 000Д. В качестве других факторов роста для фибробластов называют соматотропин, соматомедины, инсулиноподобные пептиды, инсулин, глюкагон. Важную роль в пролиферативных явлениях играют кейлоны - термолабильные гликопротеины с молекулярной массой 40 000Д, способные ингибировать клеточное деление путем инактивации ферментов, участвующих в редупликации ДНК. Одним из основных источников кейлонов являются сегментоядерные нейтрофилы. По мере снижения количества нейтрофилов в очаге воспаления уменьшается содержание кейлонов, что приводит к ускорению деления клеток. По другим предположениям, при воспалении сегментоядерные нейтрофилы практически не вырабатывают кейлоны и усиленно продуцируют антикейлоны (стимуляторы деления); соответственно деление клеток ускоряется, пролиферация усиливается. Другие клетки и медиаторы могут модулировать репаративный процесс, воздействуя на функции фибробластов, макрофагов и лимфоцитов. Существенное значение в регуляции репаративных явлений, по Д.Н. Маянскому, имеют также реципрокные взаимоотношения в системе коллаген - коллагеназа, стромальнопаренхиматозные взаимодействия. Пролиферация сменяется регенерацией. Регенерация не входит в комплекс собственно воспалительных явлений, однако непременно следует им и трудно от них отделима. Она состоит в разрастании соединительной ткани, новообразовании кровеносных сосудов, в меньшей степени - в размножении специфических элементов ткани. При незначительном повреждении ткани происходит относительно полная ее регенерация. При образовании дефекта он заполняется вначале грануляционной тканью - молодой, богатой сосудами, которая впоследствии замещается соединительной тканью с образованием рубца. 8. Признаки воспаления: Местные:покраснение, припухлость, жар, боль, нарушение функции Общие: лейкоцитоз, изменение лейкоцитарной формулы, увеличение СОЭ, изменение белкового состава крови, лихорадка, ухудшение самочувствия. Стадии развития воспаления: 1. Альтерация (повреждение): высвобождение БАВ (биологически активных веществ), расширение капилляров, повышение проницаемости сосудистой стенки, развитие ацидоза. Артериальная гиперемия 2. Экссудация: пропотевание из сосудов в ткани жидкой части крови с находящимися в ней веществами, а также клеток крови. Сдавливание и тромбирование венул приводит к остановке тока крови (стаз), происходит замедление и прекращение лимфооттока, что способствует изоляции очага воспаления 3. Пролиферация- процесс размножения клеток - завершающая стадия воспаления Исход воспаления: 1.Полное восстановление ткани 2. Образование молодой грануляционной ткани→волокнистая зрелая соединительная ткань (рубец) Формы воспаления: Классификация по характеру экссудата: 1. Острое и хроническое 1. Катаральное воспаление – в экссудате много 2. Банальное слизи 2. Специфическое –воспаление, вызванное 2. Гнойное возбудителями туберкулёза, сифилиса, проказы 3. Фибринозное 4. Геморрагическое ВИДЫ ВОСПАЛЕНИЯ И ИХ ПРИЗНАКИ 1. Серозные виды воспаления. Оно начинает появляться из-за каких-либо механических и химических травм, а так же обморожений. Этот вид воспаления воспаления зачастую появляется в слизистых кожного покрова, чуть резе во внутренних органах человека;. Геморрагические . Зачастую оно появляется в слизистых верхних дыхательных путей. Воспаление проявляется при возникновении в человеческом организме вируса гриппа. Он в свою очередь способствует пропотеванию некоторых сосудов и постепенному накоплению болезнетворных бактерий; Фибринозные . Зачастую он возникает при образовании экссудата, который имеет большое количество фибриногена. Он в свою очередь в пораженной ткани становится фибрином. Данное воспаление необходимо лечить еще на начальной стадии, так как оно становится первопричиной возникновения других заболеваний; Гнойные . При этом виде воспаления воспаления появляется в экссудате значительное преобладание нейтрофилов. При распаде они становятся гноем или так называемыми гнойными тельцами. В жидкости, что они образуют, появляются так же лимфоциты, микроорганизмы и мертвые клетки ткани. Гной получается в виде мутной и густой жидкости, которая имеет желтый цвет, с оттенками зеленого. Следует отметить то, что гнойное воспаление может возникнуть в любом органе или ткани; Катаральные . При данном воспалительном процессе происходит выделение большого количества экссудата, а так же отекает слизистая оболочка. Ощущение этого воспаления можно сравнить лишь с кусочком горького перца, если поместить его в ротовую полость. Многие характеризуют признаки воспаления как прикосновение языка к прогретому железу; Смешанные . Одно из наиболее неприятных воспалений. Оно состоит из комплекса включающего вышеописанные виды воспаления. Причем признаки воспаления могут подходить сразу к нескольким видам воспалительных процессов. Следует так же отметить, что воспаление может возникнуть в любой части организма. 10. Хронические типы воспаления: признаки и причины Хронические типы воспаления - это процесс более длительный, при котором альтерация, в отличие от острого воспаления, выражена менее ярко. Происходит реакция тканей, с инфильтрацией мононуклеарных клеток. Причины воспаления хронической формы болезни: инфекционные заболевания, такие как туберкулез, сепсис, сифилис и др. как причины воспаления ; хронические интоксикации, такие как интерстициальный нефрит, и прочие интерстициальные заболевания легких как причины воспаления ; заболевания хронического характера с иммунным патогенезом как причины воспаления (миокардит Абрамова- Фидлера) Причины воспаления, преобразованного из острой формы болезни в хроническую: острое воспаление, которое систематично повторяется; изначальная хронизация ( что бывает редко) ; продолжительное воздействие причин воспаления; Основная особенность в том, что признаки воспаления различаются по степени активности. Для того чтобы обезвредить различные негативные воздействия, организм проявляет защитную реакцию, проявляющуюся в виде воспаления разного типа. Основным источником, а точнее местом для проникновения в организм инфекций, являются поврежденные участки кожи. Для того, чтобы уничтожить возбудителей, организм направляет в место поражения лейкоциты и компоненты плазмы. Признаки воспаления острого типа: увеличивается количество мигрирующих лейкоцитов в место возникновения воспаления; гиперемия, то есть при увеличении количества притока крови к капиллярам их стенки расширяются; так как возрастает проницаемость капилляров, то в связи с этим происходит выход белков, жидкостей из сосудов, повышая при этом осмотическое давление; усиливается приток крови; Следовательно, при повышенной проницаемости стенок капилляров, происходит выход различных клеток, жидкостей в ткань. В зависимости от этапа воспаления, чередуются типы клеток берущих участие в процессе нейтрализации неблагоприятных агентов. Так, изначально больше всего принимают участие нейтрофилы, но далее прибывают моноциты, лимфоциты. Типы воспаления взаимосвязаны друг с другом, так как при невозможности организма освободится от возбудителей инфекции острое воспаление перетекает в хроническое. 11.Исходы воспаления На процесс воспаления могут влиять многие факторы, включая природу и интенсивность повреждения, местный и тканевый ответ, а также реактивность организма, но все виды острого воспаления могут иметь, как правило, только один из трех вариантов исхода: - разрешение. В идеале однажды начавшаяся воспалительная реакция после нейтрализации и элиминации повреждающего агента должна завершаться полным восстановлением участка, в котором было острое воспаление. Такое развитие событий является обычным исходом при ограниченном воспалении либо при незначительном повреждении ткани и разрушении паренхиматозных клеток. Разрешение включает удаление макрофагами клеточного детрита и микробов и резорбцию отечной жидкости лимфатическими сосудами; - заживление путем замещения соединительной тканью (фиброза). После существенного разрушения ткани, когда воспаление развивается в ткани, не способной к регенерации, или при наличии в ткани либо в серозных полостях (плевральной, брюшной) обильного фибринозного экссудата, который не может быть полностью удален, соединительная ткань замещает поврежденный участок ткани или экссудат, преобразовывая его в фиброзную массу. Этот процесс также называют организацией; - прогрессирование процесса из острого воспаления в хроническое или развитие хронического воспаления с самого начала. Острое воспаление переходит в хроническое, если не может разрешиться вследствие персистенции повреждающего агента или нарушения процесса заживления. Биологическое значение воспаления Нарушение любого из звеньев воспалительного процесса приводит к тяжелым последствиям: возрастает риск инфекционных заболеваний, увеличивается вероятность генерализации инфекционного процесса с формированием очагов повреждения во многих органах и тканях; снижается устойчивость организма к повреждающим воздействиям факторов окружающей среды; достоверно уменьшается продолжительность жизни. Воспаление, особенно хроническое, приводит к тяжелому повреждению — местному и системному. Местное повреждение связано с расстройством микроциркуляции и высвобождением из лейкоцитов активных метаболитов кислорода и лизосомальных ферментов. Системное нарушение обусловлено развитием так называемого ответа острой фазы, который обсуждается в специальном разделе. Патофизиологические принципы противовоспалительной терапии. Этиотропное лечение подразумевает устранение, прекращение, уменьшение силы и длительности действия на ткани и органы флогогенных факторов. С этой целью применяют, например, антибактериальные препараты. Патогенетическое лечение имеет целью блокирование механизма развития воспаления. При этом воздействия направлены на разрыв звеньев патогенеза воспаления, лежащих в основе, главным образом, процессов альтерации и экссудации. Для этого используют, например, антигистаминные препараты, глюкокортикоиды, ингибиторы циклооксигеназ. Саногенетическая терапия направлена на активацию общих и местных механизмов компенсации, регенерации, защиты, восстановления и устранения изменений в тканях и клетках, вызванных флогогенным агентом. Симптоматическое лечение. Мероприятия, направленные на предупреждение или устранение неприятных, тягостных, усугубляющих состояние пациента симптомов (с этой целью применяют, например, анестезирующие ЛС, вещества, способствующие нормализации функций органов и физиологических систем).