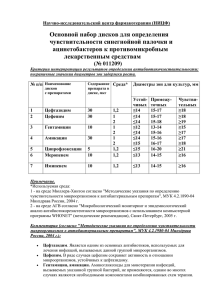
Современные проблемы антибактериальной терапии: Э.А. Ортенберг Тюменская медакадемия
реклама

Современные проблемы антибактериальной терапии: Э.А. Ортенберг Тюменская медакадемия ЖУРНАЛ «КЛИНИЧЕСКАЯ МИКРОБИОЛОГИЯ И АНТИМИКРОБНАЯ ХИМИОТЕРАПИЯ» • Официальный журнал МАКМАХ • Издается ежеквартально с 1999 г. • Рецензируется и входит в перечень ВАК • 100 страниц информации: оригинальные статьи, руководства, обзоры • Подписные индексы: Каталог «Газеты. Журналы»: 82125 – для индивид. подписчиков; 82126 – для организаций Каталог «Пресса России»: 38290 – для индивид. подписчиков; 38041 – для организаций АБ - ЖНВЛС • • • • • • • • • • • • • • • Азитромицин Амикацин Амоксициллин Амоксициллин + клавулановая кислота Ампициллин Бензатин бензилпенициллин Бензилпенициллин Ванкомицин Гентамицин Доксициклин Кларитромицин Ко-тримоксазол Левофлоксацин Линезолид Линкомицин • • • • • • • • • • • • • • • • • Меропенем Нитрофурантоин Оксациллин Офлоксацин Сульфацетамид Феноксиметилпенициллин Фуразидин Хлорамфеникол Цефазолин Цефепим Цефоперазон Цефотаксим Цефтазидим Цефтриаксон Цефуроксим Ципрофлоксацин Эритромицин Современные проблемы антимикробной химиотерапии • Рост резистентности – Нозокомиальных возбудителей Снижение эффективности – В популяции • Нерациональное использование антибиотиков – Чрезмерное назначение – Неадекватный выбор – Низкие дозы Рост резистентности • Широкое использование генериков низкого качества – ципрофлоксацин, амикацин и др. Рост резистентности Результат бактериологического исследования Пациент К, диагноз: НПивл, источник – БАЛ Результат: Pseudomonas aeruginosa 108 КОЕ/мл Пиперациллин Пиперациллин/тазобактам Цефтазидим Цефепим Имипенем Меропенем Гентамицин Амикацин Ципрофлоксацин R R R R R R R R R Конец эры антибиотиков ?! Происхождение антибиотикорезистентности • Спонтанные мутации • Селекция резистентных штаммов – «контакт с антибиотиком» Современные проблемы антибиотикорезистентности в стационаре • • • • • Стафилококки Резистентность к метициллину (оксациллину) - MRSA Резистентность к ванкомицину - VISA Энтерококки Резистентность к ванкомицину - VRE Enterobacteriaceae Резистентность к цефалоспоринам III – БЛРС Pseudomonas aeruginosa Полирезистентность Причины неадекватности терапии • Назначение неадекватного антибиотика – Природная устойчивость – Приобретенная устойчивость • Формирование устойчивости в процессе терапии • Выбор неадекватного режима дозирования Резистентность микроорганизмов • Природная (генетическая) – Микоплазмы к бета-лактамам – Грамотрицательные бактерии к бензилпенициллину • Приобретенная – Мутации • Возникновение при контакте с антибиотиком • Селекция устойчивых клонов – Горизонтальный (плазмидный) перенос (обмен) факторов резистентности – Экспрессия факторов резистентности на фоне лечения Механизмы резистентности • Ферментативная инактивация антибиотика – Бета-лактамазы – Аминогликозид-модифицирующие ферменты • Модификация мишени действия – Пенициллинсвязывающие белки (ПСБ) • Устойчивость стафилококков к оксациллину • Устойчивость пневмококков к пенициллину • Нарушение проницаемости внешних структур микробной клетки – Грам(-) бактерии • Активное выведение антибиотика из микробной клетки (эффлюкс) Эффективность антибиотика • Определяется минимальной концентрацией, способной подавлять патогенные микроорганизмы, входящие в спектр его активности (МПК) • МПК-50: подавляет рост 50% штаммов • МПК-90: подавляет рост 90% штаммов Эффект инокуляции: снижение активности антибиотика при высокой концентрации бактерий (чувство локтя) Критерии оценки антибиотика • • • • терапевтическая эффективность безопасность экономическая эффективность предотвращение селекции штаммов патогенов, устойчивых к антибиотикам резерва • удобство для пациента Управление антибиотикотерапией Классификация антимикробных средств • С преим. действием на Гр+ флору • С преим. действием на Гр- флору • Широкого спектра действия Внутри каждой группы – препараты с преимущ. влиянием на аэробов или анаэробов 06.05.2016 Ed. Ort. 34 Связь эффекта антибиотика с временем и концентрацией • «Времязависмые» антибиотики (В-лактамы, макролиды): уровень в крови выше МПК-90 – не менее 16 часов в сутки • «Концентрациязависимые антибиотики (аминогликозиды, фторхинолоны, азалиды): эффект пропорционален высоте концентрации (пусть даже кратковременной) Стрептококки • Фарингит, скарлатина, кожные инфекции, ревматизм, эндокардит, гломерулонефрит • Пневмококк – внебольничная пневмония • Альфа-гемолитический (зеленящий) – полость рта • Энтерококки – нозокомиальная инфекция (цефалоспорины неэффективны). Катетеры Грампозитивные анаэробы • Клостридии – 80 видов (газовая гангрена, токсикоинфекции, столбняк, ботулизм) • Cl. difficile – псевдомембранозный колит • Актиномицеты: лицо, грудная, брюшная полости • Пептококки, пептострептококки – полость рта Стафилококки • Патогены: aureus, epidermitis, saprophyticus • Обусловливают инфекцию любой области (с-м Лайелла) • Обычная инфекция –эндогенная или нозокомиальная • S. aureus- возможна коагуалазная активность • S.epidermitis:протезы,дренажи, катетеры • S.saprophiticus- гениталии,уретра Антибиотики с преимущ. влиянием на Гр+ флору • • • • • • • «Классические» пенициллины Макролиды Линкозамиды Гликопептиды Оксазолидиноны Рифамицины Препараты разных групп Основные мишени В-лактамов ПСБ: транспептидазы, карбоксипептидазы ПСБ-1: ПСБ-2: ПСБ-3: 06.05.2016 общий рост клетки форма клетки образование перегородки (деление) Ed. Ort. 40 Бензилпенициллин • Бактерициден • Активность против стрептококков (энтерококки – слабо), трепонем, анаэробов • Препарат выбора при тонзиллитах (БГСА) • Неактивен против стафилококков • Аллергогенен • Парентеральное применение – стационар 06.05.2016 Ed. Ort. 41 Основные возбудители внебольничной пневмонии В половине случаев возбудитель установить не удаётся. В случае идентификации: • Пневмококк - 30-50% • Гемофильная палочка (ХОБЛ) - 5-20% • Микоплазма, хламидии - молодые больные -20-30%, старший возраст - 5% • S. аureus - 5% АБТ стрептококкового ИЭ •4 недели: Ампициллин 2 г 6 р в сутки + гентамицин (как при остром ИЭ) •4 недели: Бензилпенициллин 3-4 млн ЕД 6 р в сутки + гентамицин (как при остром ИЭ) (при низкой МПК возможна монотерапия) •4 недели: Цефтриаксон 2 г 1 р в сутки + гентамицин (как при остром ИЭ) или + нетилмицин 4 мг/кг 1 р в сутки (при низкой МПК возможна монотерапия) •4 – 6 недель: Ванкомицин 30 мг/кг/сутки (в 2 введения) + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (высокая МПК, аллергия на В - лактамы) Помощь при анафилактическом шоке на БП • Эпинефрин (адреналин) – по 0,2 мл в 2-3 участка • ГКС быстрого действия • Плазмозаменители • Антигистаминные 1 поколения Если в анамнезе –анафилактический шок на пенициллин, другие В-лактамы тоже вводить нельзя 06.05.2016 Ed. Ort. 44 Оксациллин • Мишень – стафилококки (MSSA), при стрептококковых инфекциях нецелесообразен • При MRSA – бесполезен (как и все остальные В-лактамы) • Антибиотик стационара • Вводить парентерально в больших дозах • Контроль функции печени Микробиологическая проблема грамположительной резистентной флоры S.рyogenes (Sпен) Sпен стрептококки энтерококки стафилококки S.pneumoniae Sамп Rпен,Sван Rамп,Sван Rван(VRE) Sмет Rмет Sокс Rокс (MRSA) Iпен,Sцс3 Rмет Iван (GISA) ванкомицин Л И Н Е З О Л И Д Этиология ИДП Возбудитель ВП ХБ Сину(обост) сит + + ОСО Фари нгит + - S.pneum. + H.Influenzae + + + + - Moraxella catarr. - + + + - S.pyog. - - - - + M.рneum + - - - - C.рneum + - - - - Legionella spp. + - - - - Спектр возбудителей в мокроте детей с хроническими бронхолегочными заболеваниями (%) 4 35 61 H. influenzae S. pneumoniae M. catarrhalis Е. В. Середа, Институт педиатрии РАМН Микоплазмы, уреаплазмы, хламидии • • • • • • • • Микоплазмы – 12 видов M. pneumoniae – 20% всех пневмоний, ЦНС M. hominis – урогенитальные инфекции Уреаплазма – негонококковые уретриты (50% у мужчин) Хламидии – только внутриклеточно! Орнитоз C. pneumoniae – пневмонии. Астма? А/склероз? C. trachomatis – трахома, уретриты Все – прокариоты. В-лактамы не работают, нет пептидогликана 06.05.2016 Ed. Ort. 49 АБТ пневмонии • Внебольничная – а) нетяжелая: амоксициллин, макролиды, доксициклин Микробиологическая диагностика нецелесообразна - б) тяжелая (или больные > 60 лет или с сопутств. заболев): макролиды + ЦС 2-3, ФХ, БП? • Госпитальная: – Аспирационная: АГ, линкозамиды, защищ. В-лактамы – В ОРИТ: карбапенемы, ЦС 3-4 + АГ 06.05.2016 Ed. Ort. 50 Бакпосев: мокрота, гемокультура Антибиотики в амбулаторной практике при пневмонии (Москва, 2002) • • • • • • • • Рекомендуемые* Амоксициллин Амоксициллин/клавуланат Цефуроксим аксетил Левофлоксацин Моксифлоксацин Эритромицин Кларитромицин Азитромицин * BTS, ERS, IDSA, Россия ** ТОР 6 (Москва) • • • • • • Назначаемые** Гентамицин Бисептол Ципрофлоксацин Азитромицин Ампиокс Ампициллин Классификация макролидных антибиотиков по химической структуре 14-членные 15-членные (азалиды) 16-членные Природные Полусинтетические Природные эритромицин олеандомицин азитромицин мидекамицин джосамицин спирамицин Полусинтетические Полусинтетические рокситромицин кларитромицин диритромицин флуритромицин мидекамицина ацетат (миокамицин) рокитамицин Роль макролидов в АБТ ВП (IDSA, 2003) • Без «модифицирующих факторов» - макролиды или доксициклин • При их наличии: респ. фторхинолоны или высокие дозы В-лактамов (амоксициллин 1,0 Х 3) + современные макролиды (азитромицин, кларитромицин) По А.И. Синопальникову, 2004 «Модифицирующие факторы» ВП • • • • • • > 65 СД ХСН ХОБЛ Алкоголизм Опухоли • Предшествующая АБТ • Предш. госпитализация • Дифф. поражения печени, почек Макролиды в комбинированной АБТ ИДП • Внебольничная пневмония (госпитализация): ЦС 2-3 + МЛ на 2-5 дней < пребывание в стационаре (J. Trowbridge et al., 2002) • В сравнении с монотерапией ЦС – при ВП летальность < в 1,5 раза (P.Gleason et al., 1999) • Макролиды + цефтриаксон при ВП: на 30-60% ниже риск летального исхода, на 0,:-1,5 дня – время пребывания в стационаре, на 1800-3400$ - прямые расходы (R. Brown et al., 2003) Комбинирование азитромицина (в/в) при ИДП • Парентеральная форма (0,5 г в 250 мл за 1 час): нетяжелые ИДП, требующие госпитализации • С В-лактамами, рифампицином, аминогликозидами – аддитивный эффект • Нецелесообразно – с линкозамидами, хлорамфениколом (идентичность механизма, перекрестная резистентность) По А.И. Синопальникову, 2004 Бактерицидный и бактериостатический эффекты макролидов Обычно - бактериостатики: большой разрыв между задерживающей рост и подавляющей концентрацией Бактерицидны в отношении: БГСА, пневмококка, возбудителей коклюша и дифтерии Антибиотики «среднетяжелых» инфекций Дополнительные эффекты макролидов • Противовоспалительный – – – – Супрессия цитокинов Стимуляция апоптоза Снижение бронхиальной секреции (Cl- каналы) Блок активности NF-каппа фактора • Модификация факторов вирулентности возбудителей, препятств.образованию биопленок • Захват нейтрофилами • Постантибиотический • Суб-МПК • Низкодозовая длительная терапия диффузного панбронхиолита Внутриклеточное накопление антибиотиков Соотношение внутри/внеклеточной концентрации: МАКРОЛИДЫ > 10 ТЕТРАЦИКЛИНЫ, АМИНОГЛИКОЗИДЫ, ФТОРХИНОЛОНЫ 1-10 -ЛАКТАМЫ, МЕТРОНИДАЗОЛ <1 Кларитромицин - клиническая эффективность Обобщенные результаты лечения 2556 больных с различными респираторными инфекциями. (Bogossian M., 1995) Хорошие 21% Неопределенные 1% Удовлетворительные 2% Отрицательные 1% Отличные 75% Кларитромицин - переносимость лечения Bogossian M.,1995 Хорошая 27% Удовлетворитель ная Неопределенная 3% 1% Плохая 1% Отличная 68% Современная тенденция – назначение кларитромицина с замедленным высвобождением (SR) Резистентность к макролидам • Активное выведение (М-фенотип) – синтез транспортного белка: низкий уровень резистентности • Метилирование аденина в рибосомах: (MLS – фенотип) – высокий уровень резистентности • Точечные мутации – непредсказуемая индивидуальная резистентность к отдельным антибиотикам Диспропорция между растущей резистентностью и сохраненной клинической эффективностью Фармакодинамика бета-лактамов и макролидов • Предиктор эффективности: Т > МПК90 Время, в течение которого концентрации антибиотика в крови превышают значения МПК90 для возбудителя • Условие достижения гибели бактерий: Т > 50% интервала дозирования Концентрации антибиотика должны превышать значения МПК90 по крайней мере в течение половины интервала между приемами/введениями Возможность контроля распространения устойчивости к макролидам Опыт Финляндии • Снижение потребления макролидов с 2,4 сут.доз/1000 в 1991 г. до 1,38 в 1992 г. и далее Снижение частоты устойчивости S,pyogenes к эритромицину с 16,5% в 1992 до 8,5% в 1998 [Seppala H. N Engl J Med 1997;337:441] Опыт Японии • Частота S.pneumoniae MR снизилась с 62 до 3% после сокращения потребления эритромицина с 170 до 85 т в год [Fujita K, et al. Pediatr Infect Dis J 1994; 13: 1075-8] Принципиальные отличия азалидов (азитромицин) от других макролидов • Концентрационно-зависимая эффективность • Более активное поступление в ткани • Высокая активность против H. Influenzae • Лучше всасывается • Длительно действует • Короткий курс лечения Азитромицин и муковисцидоз • Длительное введение низких доз: – cнижает вирулентность P. aeruginosa Reinert P, 1995 – несколько повышает ОФВ1 Carr RR, Nahata MC. 2004 – cнижает число обострений Saiman L et al., 2003 – улучшает качество жизни и < уровень СРП Wolter J et al., 2002 Требуются дальнейшие исследования Линкосамиды (линко-, клиндамицин) • • • • Антианаэробный эффект Хорошо проникают в костную ткань Действуют на MSSA, стрептококков Более токсичны, чем В-лактамы и макролиды • Часто – псевдомембранозный колит • MLS-резистентность 06.05.2016 Ed. Ort. 68 Гликопептиды (ванкомицин, тейкопланин) •Основной объект - метициллинрезистентный S. aureus (MRSA) - «жизнеспасающий эффект» •Влияние на конечные этапы синтеза пептидогликана •Режим дозирования: 1 г / 500 мл через 12 часов в/в медленно! в течение не менее 1 часа •Желателен контроль концентрации препаратов в крови •Аллергогенность, ото- и нефротоксичность; не сочетать с ото- и нефротоксинами •У беременных, детей до 3 лет – по жизненным показаниям Ванкомицин – преимущества и ограничения •Большой опыт применения •Низкий уровень развития резистентности (связана с модификацией дипептида клеточной стенки) •Относительно недорогой препарат •Бактериостатический эффект •Аллергогенность, нефротоксичность (особенно в сочетании с аминогликозидами) – ИЭ и почки •Только парентеральный путь •Низкое проникновение в вегетации (эндокардит) (Perry J. et al, 1999) •Нарастание числа VRE (экспрессия оперона VanD) (Lefort A. et al., 2003) АБТ стафилококкового ИЭ •Метициллинчувствительные •4 – 6 недель: Оксациллин 2 г 6 р в сутки или цефазолин 2 г 3 р в сутки + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (При ИЭ искуственных клапанов + рифампицин 0,3 2 р в сутки) •4 – 6 недель: Ванкомицин 30 мг/кг/сутки (в 2 введения) + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (высокая МПК, аллергия на В - лактамы) •Метициллинрезистентные •4 – 6 недель: Ванкомицин 30 мг/кг/сутки (в 2 введения) + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (высокая МПК, аллергия на В - лактамы) АБТ энтерококкового ИЭ •4-6 недель: Ампициллин 2 г 6 р в сутки или Бензилпенициллин 4-5 млн ЕД 6 р в сутки + 2 недели гентамицин (при низкой МПК возможна монотерапия) •4-6 недель: Амп/сульбактам 3г 4 р в сутки + гентамицин или ванкомицин (продуцент В-лактамаз) •4 – 6 недель: Ванкомицин 30 мг/кг/сутки (в 2 введения) + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (высокая МПК, аллергия на В - лактамы) •4-6 недель: Линезолид 0,6 2 р в сутки (риск нефротоксичности, резистентность к ванкомицину) Энтерококк природно устойчив к цефалоспоринам Аллергия на ванкомицин Аллергия на ванкомицин Резюме по применению ванкомицина для лечения НП, вызванной MRSA • Переоценка клинической эффективности ванкомицина • ~40% случаев неэффективность ванкомицина не распознается клиницистами • Основное заблуждение: если нет эффекта от ванкомицина, значит инфекция вызвана не MRSA, а другой флорой Рифампицин • Микобактерии (туберкулез, лепра) • Устойчивые стафилококки • Хламидии, микоплазмы, анаэробы • Индуктор микросомальных ферментов 06.05.2016 Ed. Ort. 76 Препараты разных групп • Оксазолидиноны (линезолид) • Стрептограмины (синерцид) • Липопептиды (даптомицин) Линезолид (зивокс) – преимущества и ограничения •Представитель нового класса (оксазолидиноны) •Оригинальный механизм действия (препятствует образованию комплекса РНК-рибосома) •Эффективен в отношении ампициллин- и ванкомицинрезистентных энтерококков •Простая схема (0,6х2), полное всасывание из ЖКТ •Не нужна коррекция при любой степени ПН, метаболизм – без участия цитохрома Р-450 (Garsia Q. et al., 2003) •Резистентность – с 0 до 17% после 6 месяцев применения в больнице (Raad I. et al., 2004) •Способен вызывать тромбоцитопению (– вит.В6), нейропатию (обычно при очень длительном курсе) Эмпирическая АБТ подострого ИЭ у в/в наркоманов (3-створчатый клапан) •4 – 6 недель: Оксациллин 2 г 6 р в сутки или цефазолин 2 г 3 р в сутки + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (при клинической эффективности в течение 7 дней возможен 2-недельный курс) •4 – 6 недель: Ванкомицин 30 мг/кг/сутки (в 2 введения) + (2 недели) гентамицин 3 мг/кг/сутки в 2-3 введения (подозрение на резистентные стафилококки или энтерококки, аллергия к В-лактамам) •4 недели: Линезолид 0,6 г 2 р в сутки (в/в, внутрь) Осложненные ИКМТ Диагноз: целлюлит и абсцессы кожи, подкожной клетчатки, раневая инфекция Препарат: Линезолид: 600 мг х 2 р/с Оксациллин: 2 г х 4 р/с Клиническая эффективность: Линезолид: 90% Оксациллин: 85% Stevens et al. Antimicrob Agents Chemother. 2000;44:3408-3413 Основные возбудители тяжелых инфекций ИДП Кровь ИМВП Хир.И S. aureus Staph. spp. Enterococcus spp. P. aeruginosa Enterobacteriaceae Candida spp. Другие 17 2 2 16 22 4 11 40 10 3 10 5 3 2 14 11 30 15 13 14 15 10 20 5 37 20 25 24 Микроорганизмы, характеризующиеся множественной резистентностью • Pseudomonas aeruginosa • Acinetobacter spp. Pseudomonas aeruginosa (синегнойная палочка) • «Оппортунистический» патоген • «Мукоидные штаммы» наиболее вирулентны • Ограниченая потребность в питании • Продуцируемый токсин нарушает синтез белков хозяина • Имеющиеся ворсинки способствуют адгезии • Резистрентность к антибиотикам: структура, выработка лактамаз, трансфераз • Резистентность к антисептикам Перекрестная устойчивость P. aeruginosa к бета-лактамным антибиотикам Тик+клав S/r r/R R S/r Пипер S r/R r/R S Пипер+таз S r/R r/R S Цефтаз S r/R r/R S Цефепим S S/r R S Ими S S S R Меро S S r r AmpC Эффл OprD(-) Частота нечувствительных к антибиотикам (R+I) нозокомиальных штаммов P.aeruginosa в ОРИТ % 80 74 60 38 33 40 23 20 12 3 0 МЕР 6 АМИК ЦЕФТ ИМИ ЦИПР П/ТАЗ Страчунский ЛС и др. КМАХ 2003; 5 (1): 35-46 ГЕНТ Антибиотики, преимущественно активные против Гр-- флоры • • • • Аминогликозиды Фторхинолоны Монобактамы Имидазолы 06.05.2016 Ed. Ort. 86 Аминогликозиды Преимущества Антистафилококковая активность Грам-отрицательные аэробы - основная мишень Выраженная антисинегнойная активность (нозокомиальная флора) Недостатки Анаэробы - активность отсутствует Узкий терапевтический диапазон Выраженный токсический потенциал: - ототоксичность (> амикацин) - нефротоксичность (> гентамицин) - нейротоксичность Позиционирование антибиотиков в стационаре: актуальные потребности Аминогликозиды • Гентамицин – Стафилококки – в сочетании с оксациллином или ванкомицином – Энтерококки – в сочетании с ампициллином или ванкомицином – По другим показаниям исключить • Амикацин – Только ОРИТ ( в других отделениях – исключить) – Основное показание – в сочетании с цефалоспоринами при псевдомонадных инфекциях • Другие аминогликозиды преимуществ не имеют? Монотерапия бета-лактамом в сравнении с комбинацией бета-лактам + аминогликозид при сепсисе: метанализ рандомизированных исследований • • • • Не выявлено различий в: Летальности (ОР 0.90, 95% ДИ 0.77-1.06) Частоте бактериальной суперинфекции/колонизации Частоте фунгальной суперинфекции/колонизации Частоте развития устойчивости Комбинированная терапия не имела преимуществ по сравнению с монотерапией у пациентов с • Инфекциями, вызванными Грам(-) бактериями • Инфекциями, вызванными P.aeruginosa Фармакодинамические параметры Концентрация Cmax:МПК ППК:МПК МПК T>МПК 0 Время (часы) AUC = Площадь под кривой «концентрация-время» Cmax = Максимальные концентрации в плазме Однократное и трехкратное введение гентамицина (5 мг/кг) Концентрация (мкг/мл) 14 однократное трехкратное 12 10 8 6 4 2 0 0 4 8 12 16 20 24 Часы Nicolau et al. Antimicrob Agents Chemother 1995;39:650–655 Аминогликозиды: зависимость соотношения Cmax:МПК и клинического эффекта Клинический эффект (%) 100 83 80 65 60 89 92 10 12 70 55 40 20 0 2 4 6 8 Cmax :МПК Moore et al. J Infect Dis 1987;155:93–99 Классификация хинолонов/фторхинолонов Поколение Препарат Спектр активности I – нефторированные хинолоны Налидиксовая Г(-) флора (семейство кислота Enterobacteriaceae) Оксолиновая кислота Пипемидовая кислота II – «грамотрицательные» фторхинолоны Норфлоксацин Ципрофлоксацин Пефлоксацин Офлоксацин Ломефлоксацин Г(-) флора, S.aureus, низкая активность против S.pneumoniae и атипичных возбудителей III – «респираторные» фторхинолоны Левофлоксацин Спарфлоксацин Г(+), Г(-), атипичные возбудители IV – «респираторные» + «антианаэробные фторхинолоны Моксифлоксацин Г(+), Г(-), атипичные возбудители + высокая активность против анаэробов Механизм действия фторхинолонов Г(-) ТопоизомеразаII Двойная спираль ДНК ТопоизомеразаIV Грам(+) Суперспирализация ДНК Фторхинолоны • В случае применения ципрофлоксацина при нозокомиальной пневмонии, значения AUC:МПК >125 позволяют достигнуть клинической эффективности и эрадикации >80% • В случае применения левофлоксацина и гатифлоксацина при внебольничной пневмонии, значения AUC/МПК >34 повышают вероятность эрадикации S.pneumoniae Forrest et al. Antimicrob Agents Chemother 1993;37:1073–1081 Ambrose et al. Antimicrob Agents Chemother 2001;45:2793–2797 Активность фторхинолонов в отношении S.pneumoniae (Monte Carlo analysis) Быстрый рост резистентности нозокомиальной флоры Вероятность достижения AUC/МПК > 30 – Ципрофлоксацин 3% – Левофлоксацин 78% – Гатифлоксацин 98% – Моксифлоксацин 98% [Owens RC, et al. 40th ICAAC, 2000] Рекомендуемые алгоритмы (внебольничная пневмония) При легком течении - амбулаторное лечение Препараты выбора:аминопенициллины современные макролиды Альтернатива: защищенные пенициллины респираторные фторхинолоны При тяжелом течении - госпитализация Л. С. Страчунский, 2002 В. К. Таточенко, 2000 Программа антибактериальной терапии тяжелой внебольничной пневмонии Схема 2 Фторхинолон II поколения в/в • Моксифлоксацин 400 мг • Левофлоксацин 500 мг – – – – S.pneumoniae PS+PR S.aureus K.pneumoniae Legionella, C.pneumoniae Позиционирование антибиотиков в стационаре: актуальные потребности Фторхинолоны Ранние • С антисинегнойной активностью – ципрофлоксацин – Только ОРИТ – Исключить по другим показаниям • Без активности против P.aeruginosa – пефлоксацин офлоксацин, – Вне ОРИТ – Не средства стартовой терапии (ИМВП, пневмония, перитонит) Новые • Моксифлоксацин – тяжелая внебольничная пневмония, нозокомиальная пневмония вне ОРИТ • Левофлоксацин – инфекции КиМТ, пневмония вне ОРИТ Проникновение АБ в желчевыводящие пути, ткань pancreas • Достаточное (выше MIC): - цефалоспорины 3-4, ЦС, карбапенемы, фторхинолоны • Ограниченное:: аминопенициллины • Концентрация моксифлоксацина в pancreas существенно выше, чем в крови (Wacke R. et al., Chemotherapy, 2003), Schwab D et al., Aliment Pharmacol Ther. 2005, 22(5). • Проблемы оценки: небольшое число больных, их контингент, различия методов взятия проб, контаминация желчью Kramer K., Levy H. Pharmacotherapy 1999, 5 Shriklande S. et al. Fnim Ag Chemother, 2000, 44, 9 Биодоступность и эффективность АБ 2 • При введении тяжелым больным в ОРИТ одинаковых доз концентрация в крови имипенема в 2 раза выше, чем меропенема (AUC, peak) (Novelli A et al., Clin Pharmacokinet. 2005;44(5):539-49) • Длительная инфузия тикарциллина/клавуланата больным на дому – высокий эффект (Munckhof WJ et al., Int J Antimicrob Agents. 2005 Jun;25(6):514-22) • Биопленки: МIС существенно не возрастает для ципрофлоксацина, меропенема и возрастает для цефтазидима, тикарциллина/клавуланата, пиперациллина/тазобактама (Moskowitz SM et al., J Clin Microbiol. 2004 May;42(5):1915-22) Пефлоксацин ШИРОКИЙ СПЕКТР ДЕЙСТВИЯ, ДЕЙСТВИЕ НА МИКРООРГАНИЗМЫ УНИКАЛЬНАЯ ФАРМАКОКИНЕТИКА (БИОДОСТУПНОСТЬ, ВЫВЕДЕНИЕ) НАЛИЧИЕ ПЕРОРАЛЬНЫХ И ПАРЕНТЕРАЛЬНЫХ ФОРМ ОТЛИЧНАЯ КЛИНИЧЕСКАЯ ЭФФЕКТИВНОСТЬ ПРИ РАЗНООБРАЗНЫХ ИНФЕКЦИЯХ Антибиотики ШСД и сниженный иммунитет (онко-, гематология) Бактерицидный эффект! • Бактериемия в онкогематологии (266 больных):>> эффективен цефоперазон/ сульбактам, пиперациллин/тазобактам, имипенем (Wang FD Chemotherapy. 2005 May;51(2-3):147-53) • Онкопатология с нейтропенией: моксифлоксацин эффективен в 91% случаев (Chamilos G et al., Cancer. 2005 Jun 15;103(12):2629-35) • Нейтропеническая лихорадка: эффект имипенема – 42% (Sanz MA et al., Curr Med Res Opin. 2005 May;21(5):645-55) Антибиотики ШСД • • • • • Пеницилллины Цефалоспорины Карбапенемы Тетрациклины Хлорамфеникол Клинические особенности «базовых» антибиотиков ШСД •Ампициллин: плохо всасывается из ЖКТ, менее активен против H. Influenzae, активен против энтерококков •Амоксициллин: лучше всасывается, активен против Н.influenzae •Аминопенициллины малоактивны в отношении кишечной флоры (но подавляют E. coli) •Частые НЭ – диспепсические расстройства К каждому – высок уровень резистентности Позиционирование антибиотиков в стационаре: актуальные потребности Пенициллины • Ампициллин – Только внебольничная пневмония и эндокардит • Оксациллин – Только стафилококковые инфекции • Антипсевдомонадные незащищенные – Исключить Возможности антибактериальной терапии энтерококковых инфекций Enterococcus faecalis Чувствительный к ампициллину • Ампициллин (8-12 г/с) – При тяжелых инфекциях (+ гентамицин) • При мочевых инфекциях - нитрофураны Устойчивый к ампициллину • Ванкомицин +/- гентамицин • Линезолид Цефалоспорины неэффективны Защищенные аминопенициллины (АК, АС) АК: Эффективность при вторичном перитоните ~ имипенему, экономия – 900 € на 1 случай (Genne D, et al. Dig Surg. 2003;20(5):415-20) АС:79 рандомизированных исследований: эффективность - 87%, что совпадало с таковой у карбапенемов (Holzheimer RG, Dralle H Eur J Med Res. 2001 Jul 30;6(7):277- 91) Амоксициллин/клавуланат (АК) • По влиянию на анаэробов не уступает метронидазолу и имипенему и превосходит линкозамиды и левофлоксацин Koeth LM, et al. J Antimicrob Chemother. 2004 Jun;53(6):1039-44. • 75% штаммов E. coli, устойчивых к АС, чувствительны к АК, в основном они продуцировали β-лактамазы типа ТЕМ Kaye KS, et al.. Antimicrob Agents Chemother., 2004 May;48(5):1520-5. • АС: эффективность в отношении Acinetobacter АК: оригинальные и генерические препараты, АС – в основном - генерики Ампициллин/сульбактам (АС) • Чувствительность до 70% МРСА Сидоренко С.В. и др.Антиб химиотер. 1995, 40(3) • Сульбактам > связывание антибиотика с PSP 2α Fasola EL, et al. J Lab Clin Med. 1995 125(2) • При аспирационной пневмонии, абсцессе легкого = цефалоспорин + клиндамицин Allewelt M, et al. Clin Microbiol Infect, 2004; 10(2) Ампициллин/сульбактам (АС)-2 • При интраабдоминальных инфекциях (метаанализ 79 ККИ эффективность АС 87% (как у карбапенемов, цефотаксим + метро-, клинда-+ тобра, ЦС2, ПТ Holzheimer RG, Dralle H. Eur J Med Res. 2001 Jul 30;6(7). • При инфицированных поражениях стоп у больных диабетом АС и АК в целом были равноэффективны линезолиду Lipsky BA, et al Clin Infect Dis. 2004, 38(1) Ампициллин/сульбактам (АС)-3 • При пневмонии, вызванной Acinetobacter (в частности, в ОРИТ), АС может быть альтернативой карбапенемам Wood GC et al. Clin Infect Dis. 2002;34(11):1425-30 • У коматозных больных на ИВЛ 3-дневный курс АС (9 г в сутки) почти в 3 раза снижал риск возникновения пневмонии Acquarolo A et al. Intensive Care Med, 2005; 31(4): 510-6. Имеющиеся генерики: сультасин, амписид «Слабости» АК и АС • АК может повреждать печень (Gresser U. Eur J Med Res. 2001 Apr 20;6(4):139-49 • При преждевременном разрыве плодного пузыря АК > частоту некротизирующего энтероколита у новорожденных, АС – нет (Lewis DF et al., 2003) • Активность защищенных В-лактамов снижает предварительное введение карбапенемов, цефалоспоринов, аминогликозидов Harris AD, et al. Antimicrob Agents Chemother, 2002, 46, 3, 854-858. Малоэффективны (как и цефалоспорины 3-4) в отношении продуцентов БЛРС Амоксициллин-клавуланат, клинические особенности При АБП - активен против энтерококков и бактероидов (в отличие от цефуроксима, цефазолина) Широко используется в педиатрии Резистентность H. influenzae возникает медленно (в отличие от макролидов) (Clark C. et al., 2002) Эффективность при вторичном перитоните ~ имипенему, экономия – 900€ на 1 случай Противопоказан при мононуклеозе (Genne D. et al., 2003) Тикарциллина клавуланат Форма выпуска •Флакон 3,2 гр № 4 (3г тикарциллина в форме натриевой соли, 200 мг клавулановой кислоты) •Предназначен для внутривенной инфузии •Эффективен: MSSA, H. infl., P. aerug., E. faecalis, St. maltophylia, Enterobact. Spp., B. fragilis •Применяется в дозе 3,2 г каждые 6-8часов Контроль электролитов, свертывания Применение тикарциллина/клавуланата для лечения тяжелых инфекций в детской клинике (7 клиник США, 317 детей) Клинический эффект достигнут у 95,9% детей: 79% у больных с внутрибрюшными инфекциями, 100% у больных сепсисом Пневмонии – 56% Инфекции опорно-двигательного аппарата – 100% Уроинфекции – 86% Инфекции ЛОР-органов – 85% Инфекции ЖКТ – 100% Blumer JL 1998 Резистентная флора Неферментирующие бактерии P. aeruginosa, Acinetobact. spp., Stenotrophomonas malt. и др. • США (TSN, 1998-2001) чувствительность P. аeruginosa – Карбапенемы: – Тикарциллин/клавуланат, ципрофлоксацин: 80-90% 70-80% • Чувствительность A. baumannii: – – – – – Имипенем: Меропенем: Тикарциллин/клавуланат: Амикацин: Цефтазидим, ципрофлоксацин: 96% 91% 80% 80% < 60% Karlowsky JA et al., Antimicrob Agents Chemother. 2003 May;47(5):1681-8. Резистентная флора Неферментирующие бактерии Stenotrophomonas maltophilia: • Наряду с псевдомонадами играет роль при муковисцидозе (Canton R et al., : Pediatr Pulmonol. 2003 Feb;35(2):99-107) • Резистентность к карбапенемам • Эффективен доксициклин, котримоксазол? • Из фторхинолонов >> – моксифлоксацин (Rolston KV et al., Diagn Microbiol Infect Dis. 2005 Mar;51(3):215-8.) • Чувствительность к тикарциллину/клавуланату – 95%, к тикарциллину – 15% (Caylan R et al., Jpn J Infect Dis. 2004 Apr;57(2):37-40 ) ЦС - 1 • Основной препарат – цефазолин • Парентерально: цефпрозил – в России не используют • Перорально: цефалексин, цефадроксил – применяют ограниченно 06.05.2016 Ed. Ort. 119 ЦС-2 • Основной препарат – цефуроксим • Другие : - парентерально: цефотетан, цефокситин, лоракарбеф – реально в России не используются • Перорально - цефаклор – применение ограниченно 06.05.2016 Ed. Ort. 120 Принципы АБП Микробная контаминация раны неизбежна (к концу операции 80-90%, чаще стафилококком) Эффективная концентрация АБ в ране должна быть от начала до конца операции АБ вводится в/в - за 30-40 мин до начала операции (первого разреза) Не следует стремиться к полной эрадикации микроорганизмов - достаточно снижения их числа Введение АБ дольше 24 часов после операции не повышает эффективности профилактики РИ Выбор антибиотиков для АБП * НЕ ИСПОЛЬЗУЮТСЯ МОНОКОМПОНЕНТНЫЕ СХЕМЫ пенициллин, ампициллин, метронидазол, гентамицин, пиперациллин, цефотаксим, тинидазол, линкомицин, левомицетин, цефалотин, эритромицин ВХОДЯТ В СХЕМЫ АБП Наиболее широко используются: цефазолин, цефуроксим Используются по специальным показаниям: - ванкомицин: MRSA, аллергия на -лактамы - амоксициллин/клавуланат, метронидазол: Bacteroides - пенициллин, доксициклин: медицинский аборт (I *триместр) F.Song, A. Glenny; Health Techn. Asses. 1998, 2,7 Л.С. Страчунский с соавт., 2002 - фторхинолоны: вмешательства на МВП и простате ЦС - 3 • Парентерально: «многоцелевые» - цефотаксим, цефтриаксон; «антисинегнойные» цефоперазон, цефтазидим, «антианаэробный» латамоксеф • Перорально: цефиксим, цефтибутен, цефпрозил – применение ограниченное 06.05.2016 Ed. Ort. 123 ЦС - 4 • Цефепим (максипим) • Антипсевдомонадная активность • Устойчивость к БЛРС 06.05.2016 Ed. Ort. 124 Позиционирование антибиотиков в стационаре: актуальные потребности Цефалоспорины • I-II поколение (цефазолин, цефуроксим) – Предоперационная профилактика • III поколение Цефотаксим, цефтриаксон – Исключить при госпитальных инфекциях – Внебольничные: пневмония, менингит, мочевые Антипсевдомонадные: цефтазидим – Только ОРИТ, только P.aeruginosa • IV поколение (цефепим) – ОРИТ, P.aeruginosa, ротация схем стартовой терапии Особенности отдельных ЦС • • • • Цефазолин: АБП, нефротоксичность Цефуроксим: АБП, гемофильная палочка Цефтриаксон: длительность, ЦНС, желчь Цефтазидим, цефоперазон: синегнойная палочка • Цефоперазон-сульбактам: ацинетобактер 06.05.2016 Ed. Ort. 126 Слайд Слайд 522 7 8 13 14 15 16 17 18 19 изиз О Предыдущий ·С ледующий главление 37 37 Принципы включени я антимикр обных препарато в в формул яр лечебнопрофилак тического учрежден ия (IX РНК "Человек и лекарство", Школа для врачей по формулярной системе) © НИИ АХ СГМА 2000, 2001, 2002 Нозокомиальная пневмония * Другие 22% P.aeruginosa 9% S.aureus 9% Enterobacter spp. 6% H.influenzae 20% K.pneumoniae 34% Необходимо назначать антибиотики широкого спектра * National Nosocomial Surveillence System Report, 1990- Нозокомиальная пневмония (НП) (Чучалин А.Г. и соавт, 2005 (КМАХ, 2005,1 • Без нарушений иммунитета • Ограничение избыточного применения антибиотиков • Снижение частоты неадекватных назначений антибиотиков • НП: ранняя – 2-5 дней от госпитализации • Поздняя – не ранее 6 дня • При поздней – выше риск полирезистентных возбудителей (ПРВ) Патогенез НП • Аспирация секрета ротоглотки!!! – – – – Нарушения сознания, седативные препараты Расстройства глотания Снижение рвотного рефлекса Угнетение двигательной активности ЖКТ • Аспирация содержимого пищевода/желудка – Ахлоргидрия – Голодание, энтеральное питание – Лекарства, снижающие кислотность • Ингаляция микробного аэрозоля • Гематогенный путь Микробиологическая диагностика НП • До начала АБТ – 2 образца крови • Строго соблюдать асептику • Основное – свободно откашливаемая мокрота • Трахеальный аспират • Основные возбудители НП: золотистый стафилококк, неферментирующие бактерии, энтеробактерии, часто они ПРВ Эмпирическая АБТ ранней НП (Чучалин А.Г. и соавт, 2005 (КМАХ, 2005,1) • Основные возбудители: – S.pneum., S.aureus, H.infl., E.coli, K.pneum, Enterobact.spp • Рекомендуемые препараты: – – – – ЦС-3 (цефтриаксон, цефотаксим) Защищенные аминопенициллины ФХ (лево-, мокси-, ципрофлоксацин) эртапенем Эмпирическая АБТ поздней НП • Основные возбудители: – P. aerug., K.pneum (БЛРС), Acinetobact., L.pneumophilia • Рекомендуемые препараты: – ЦС-3 -4 (антисинегн): цефепим, цефтазидим – Карбапенемы (ими-, меропенем) – Защищенные В-лактамы (антисинегн): сульперазон, тикарциллин-клавуланат ПЛЮС ФХ (лево-, ципрофлоксацин) или амикацин ПЛЮС линезолид или ванкомицин (риск MRSA) Факторы риска при НП • • • • • • Фактор риска Балл Возраст > 65 лет Структурные заболев. легких Предшествовавшая АБТ Позднее начало (на 5 сутки) Тяжелая ДН Органная дисфункция 1 2 2 3 3 4 K. Bodmann et al., 2004 Эмпирическая АБТ НП Балл АБТ <2 Ингибиторзащ. аминопениц, ЦС 2-3, ФХ 2-3 3-5 Антисинегн. ЦС, ФХ 2-3, карбапенемы, пипер/таз 6и> ЦС, карбапенемы, пипер/таз + ФХ 2-3 или АГ K. Bodmann et al., 2004 Неадекватная АБТ - фактор риска летальности пациентов ОРИТ Летальность (%) 60 Неадекватная АБТ Адекватная АБТ p<0.001 p<0.001 50 40 30 20 10 0 Общая Связанная с инфекцией Kollef et al. Chest 1999;115:462–474 При НП нет необходимости назначать • • • • • Иммуномодуляторы Ингибиторы протеаз Синтетические эндорфины (даларгин) Цитохром С Иммуноглобулины Антибиотики при тяжелой пневмонии Внебольничная • Цефалоспорин III-IV + макролид • Респираторные ФХ Нозокомиальная • • • • Цефтазидим Цефепим Цефоперазон/СБ Ранние и респираторные ФХ • Имипенем • Меропенем Адекватные режимы терапии госпитальной пневмонии • Вне ОРИТ (+/- аспирация) – Без предшествующих антибиотиков • ЦС III (+/- метронидазол) • Фторхинолон • Новые ФХ > ранних ФХ • Левофлоксацин +/- метронидазол • Моксифлоксацин – Предшествующие антибиотики • Ингибитор-защищенный АП бета-лактам • Цефепим Адекватные режимы терапии госпитальной пневмонии НПивл • Антипсевдомонадный бета-лактам – Цефтазидим, цефепим, имипенем, меропенем • Второй этап: + линезолид или ванкомицин • При гнойно-деструктивном процессе – цефоперазон-сульбактам Овсянкин В. И др., 2004 В-лактамазная активность нозокомиальных клинических штаммов • S. аureus – 90 – 95% • K. pneumoniae – 100% (БЛРС – 90%) • P. aeruginosa -100% • H. Influenzae - 100% • А. baumannii - 100% • Анаэробы - 40 – 100% • E. coli - 40-60% В.П.Яковлев и соавт., 2003 Клинически важные бета-лактамазы • Стафилококковые бета-лактамазы • Бета-лактамазы грамотрицательных бактерий – AmpC – Широкого и расширенного спектров (ESBL) • TEM • SHV • CTX – Карбапенемазы Практически важные свойства AmpC бета-лактамаз • Спектр активности – Гидролизуют цефалоспорины I – III поколений – Карбапенемы, цефепим сохраняют активность – Устойчивы к действию ингибиторов • Характер продукции – Индуцибельный • Enterobacter, Serratia, Morganella, Citrobacter Клиническое значение AmpC бета-лактамаз • Селекция гиперпродуцентов возможна в процессе лечения тяжелых инфекций (на фоне высокой обсемененности очагов инфекции) цефалоспоринами III поколения – Госпитальная пневмония – Бактериемия • При лечении легких и среднетяжелых инфекций селекции обычно не происходит – Инфекции мочевыводящих путей Бета-лактамазы широкого и расширенного спектров Широкий спектр • Гены локализованы на плазмидах • Чувствительны к действию ингибиторов • Гидролизуют – Природные и полусинтетические пенициллины – Цефалоспорины I-II поколения Расширенный спектр • Гены локализованы на плазмидах • Чувствительны к действию ингибиторов • Гидролизуют – Природные и полусинтетические пенициллины – Цефалоспорины I - IV поколения Частота продукции БЛРС госпитальными штаммами Klebsiella pneumoniae в Европе (MYSTIC) Turner PJ. 13th ECCMID. Clin Microb Infect 2003; 9 (6) Распространение БЛРС в России («MICROMAX», Сидоренко и соавт. 1999) Продуценты ESBL и антибиотики других групп (MYSTIC) • Ассоциированная устойчивость продуцентов ESBL к аминогликозидам и фторхинолонам МПК цефтазидима (мкг/мл) ----------------------------------------------<2 2-16 >16 ----------------------------------------------Гента (%S) 100% 13% 11% Ципро (%S) 86% 92% 47% -------------------------------------------------------------------------- Неудачи цефалоспоринов III при инфекциях, вызванных продуцентами БЛРС Частота неудач % 100 80 60 40 20 0 <1 2 4 8 МПК цефалоспоринов, мкг/мл Paterson et al, JCM. 2001 Эффективность антибиотиков при инфекциях, вызванных продуцентами БЛРС • Наибольшую эффективность проявляют меропенем и имипенем [Patterson J, 2001; Paterson D, 2002] • Эффективность цефалоспоринов и фторхинолонов варьирует – Цефалоспорины III поколения – 16,6% – Фторхинолоны – 33,3% – Цефепим – 90,9% [Яковлев СВ, Ромашов ОМ, Сидоренко СВ, 5th ECC, Rhodes, 2003] • Клиническая эффективность ингибитор-защищенных беталактамов не доказана Защищенные В-лактамы •Амоксициллин-клавуланат (амоксиклав, аугментин,) •Ампициллин-сульбактам (сультасин, амписид, уназин) •Амоксициллин-сульбактам (трифамокс) •Пиперациллин-тазобактам (тазоцин) •Тикарциллин – клавуланат (тиментин) •Цефоперазон-сульбактам (сульперазон) Расширен спектр действия, снижена приобретенная резистентность Особенности комбинации цефоперазон - сульбактам • • • • • Эффективность против Гр- бактерий, устойчивых к ЦС -3 Активность против отдельных продуцентов БЛРС (как карбапенемы). Активность против анаэробных бактерий Активность против синегнойной палочки и ацинетобактер Сохранность фармакокинетических свойств цефоперазона. В.П. Яковлев, 2003 Место цефоперазон/сульбактама в лечении госпитальных инфекций Хирургические инфекции -желчевыводящих путей -послеоперационный перитонит и абсцессы -инфицированный панкреанекроз,холецистит,холангит -интраабдоминальные инфекции Инфекции в ОРИТ -септицемия, менингит -поздняя пневмония на ИВЛ -в схемах ротации (замена ЦС III или ФХ) Инфекции у больных со сниженным иммунитетом Проблемные возбудители -Acinetobacter spp. -P.aeruginosa -Klebsiella spp и др. ESBL-продуценты Цефоперазон-сульбактам (ЦС) и карбапенемы (КП) -1 • Нефермент. (3900 изолятов): резист. к ЦС – 11%, к КП – тот же уровень Fu W. et al., 2003 •Энтеробактерии из ОРИТ: резист. к ЦС возросла с 14 до 25%; резист. клебсиелл к ЦС – 17%, к КП – 2% Chen M. et al., 2003 •P. aeruginosa: КП – резист. возросла с 20 до 40%, ЦС – осталась на уровне 20% Zhang R. et al., 2003 Карбапенемы • • • • • • • Имипенем-циластатин Меропенем Эртапенем Маленькая молекула - цвиттерион Устойчивость к В-лактамазам Связывание с ПСБ - 2 Низкий уровень эндотоксинемии 06.05.2016 Ed. Ort. 155 Карбапенемы: что проверено временем? Сверхширокий спектр действия Низкая токсичность «Жизнеспасающий эффект» Компонент стандартов лечения тяжелых инфекций Возможности монотерапии Успешная история применения (в том числе в России) Дорогостоящие антибиотики Причины эффективности карбапенемов Устойчивость к -лактамазам (включая БЛРС) Молекула - цвиттерион (мембраны) Специфичность мишени (ПСБ-2) Постантибиотический эффект Отсутствие инокулюм-эффекта Широта и мощность действия Имипенем: показания к назначению Тяжелые полимикробные заболевания интраабдоминальные инфекции инфекции мягких тканей и костей, ожоги инфекции нижних дыхательных путей Госпитальные инфекции Бактериальные инфекции у больных с нарушением иммунитета Осложненные инфекции мочевыводящих путей В случае неэффективности эмпирической терапии различными антибиотиками Позиционирование антибиотиков в стационаре: актуальные потребности Карбапенемы (имипенем, меропенем) • Наиболее надежные средства эмпирической терапии • Увеличение использования приводит к: – Элиминации резистентных штаммов Enterobacteriaceae (прежде всего, продуцентов БЛРС и АмрС бета-лактамаз) – Селекции полирезистентных штаммов P.aeruginosa на фоне имипенема Ингибитор-защищенные бета-лактамы (пиперациллин/тазобактам, цефоперазон/сульбактам) • Допустимо использование в схемах ротации • Основное показание – абдоминальные инфекции • Не целесообразны при P.aeruginosa Клинические различия карбапенемов Бактериологически: имипенем > грам (+), меропенем > грам () * Имипенем - дети до 3-х месяцев - преимущество в ортопедии, при панкреатите - возможности «ступенчатой терапии» - выше риск судорог (ингибитор рецепторов ГАМК, NMDA) Меропенем - преимущество при менингитах - возможность вводить болюсно - выше эффект в отношении P. aeruginosa * White К et al, Diagn Microbiol Infect Dis. 2001: 1 Страчунский Л.С. с соавт., 2002. Меропенем 500 мг в виде 0.5-часовой и 3-часовой инфузии Концентрация мкг/мл 100 0.5-ч 3-ч 10 MПК (4 мкг/мл) 1 0.1 0 2 4 Часы 6 8 Dandekar. ICAAC 2002 [Abstr. A-1386] Развитие резистентности к карбапенемам • Имипенем – Утрата OprD (пориновый белок - проникновение) • Частота мутаций 10-7 • МПК увеличивается с 1-2 до 8-32 мкг/мл – Клиническая неэффективность • Меропенем – Активация систем активного выведения (эффлюкс) • МПК увеличивается с 0,12-0,5 до 2-4 мкг/мл – Клиническая эффективность может сохраняться – Потеря OprD + активное выведение (эффлюкс) • Вероятность одновременной мутации 10-14 [Livermore DM. JAC 2001; 47:247, 2003] Антибактериальная терапия в абдоминальной хирургии Профилактика • Амоксициллин/клавуланат • ЦС I поколения (цефазолин) • ЦС II поколения (цефуроксим) • ЦС III поколения (цефтриаксон) (особые случаи) Абдоминальные инфекции средней тяжести (APACHE II до 13 баллов) • Амоксициллин/клавуланат • Цефуроксим (+метронидазол или клиндамицин) • ЦС III поколения (цефотаксим, цефтриаксон, цефоперазон +метронидазол или клиндамицин) • Фторхинолоны (пефлоксацин) + метронидазол Антибактериальная терапия в абдоминальной хирургии Абдоминальные и экстраабдоминальные инфекции (тяжёлые: APACHE II более 13 баллов) • Защищённые пенициллины (тикарциллин/ клавуланат, пиперациллин/тазобактам) ±аминогликозиды • Цефоперазон/сульбактам • Цефалоспорины IV поколения (цефепим) +метронидазол • Карбапенемы (имипенем, меропенем) Таблица 3. Этиотропная терапия сепсиса Микрооргани змы Средства 1-го ряда Альтернативные средства Грамположительные Staphylococcus aureus MS Оксациллин 2 г 6 раз в Линкомицин 0,6 г 3 раза в сутки сутки Амоксициллин/клавуланат 1,2 г 3 раза в сутки Цефазолин 2 г 3 раза в сутки Staphylococcus Ванкомицин 1 г 2 раза в Рифампицин 0,3-0,45 г 2 раза в сутки+ коaureus MR, сутки тримоксазол 0,96 г 2 раза в Staphylococcus сутки(ципрофлоксацин 0,4 г 2 раза в сутки) epidermidis Линезолид 0,6 г 2 раза в сутки Streptococcus viridans Бензилпенициллин 3 млн Цефотаксим 2 г 3 раза ЕД 6 раз в сутки Цефтриаксон 2 г 1 раз Имипинем 0,5 г 3 раза в сутки в в сутки сутки Streptococcus pneumoniae Цефотаксим 2 г 3 раза в Цефепим 2 г 2 раза сутки Имипенем 0,5 г 3 раза в сутки Цефтриаксон 2 г 1 раз в сутки в сутки Enterococcus faecalis Ампициллин 2 г 4 раза в Ванкомицин 1 г 2 раза в сутки +/- гентамицин сутки + гентамицин 0,24 г в 0,24 г в сутки сутки Линезолид 0,6 г 2 раза в сутки Таблица 3. Этиотропная терапия сепсиса Микроорга низмы Средства 1-го ряда Альтернативные средства Грамотрицательные K.pneumoniae Enterobacter spp., Имипенем 0,5 г 3 раза в сутки Ципрофлоксацин 0,4 г 2 раза в сутки Меропенем 0,5 г 3 раза в сутки Цефепим 2 г 2 раза в сутки Имипенем 0,5 г 3 раза в сутки Ципрофлоксацин 0,4 г 2 раза в сутки Citrobacter spp., Меропенем 0,5 г 3 раза в сутки P.vulgaris, Амикацин 1 г в сутки Serratia spp. Цефепим 2 г 2 раза в сутки Acinetobacter spp. Имипенем 0,5 г 3 раза в сутки Цефепим 2 г 2 раза в Меропенем 0,5 г 3 раза в сутки Ципрофлоксацин 0,4 г 2 раза в сутки P.aeruginosa Цефтазидим 2 г 3 раза в сутки + Имипенем 1 г 3 раза в сутки + амикацин 1 г в амикацин 1 г в сутки сутки Ципрофлоксацин 0,4 г 2-3 раза в Меропенем 1 г 3 раза в сутки + амикацин 1 г в сутки + амикацин 1 г в сутки сутки Цефепим 2 г 3 раза в сутки + амикацин 1 г в сутки Candida spp. Амфотерицин В 0,6-1 мг/кг в Флуконазол 0,4 г 1 раз в сутки сутки Адекватность АБТ и исходы сепсиса (Тюмень, 2 ОКБ) • Ретроспективный анализ 180 историй • Адекватная АБТ – 84: летальность 5,4%, пребывание в ОРИТ – 18 дней • Неадекватная стартовая – 45: летальность 16,6%, пребывание в ОРИТ – 26,4 дня • Неадекватная – 51: летальность 30%, пребывание в ОРИТ – 21 день Ушакова М.А. и др., 2005 «Старые» антибиотики ШСД • • • • • • Тетрациклины Чаще – урология (хламидии) Диспепсии, кандидоз, псевдомембр. колит, холестаз, кальций, фотодерматоз Основной препарат - доксициклин Хлорамфеникол Хорошее всасывание Сальмонеллезы? Инфекции ЦНС (пневмококк, менингококк, инфлюэнца) Анемии, невриты, серый синдром 06.05.2016 Ed. Ort. 168 Слайд Слайд 534 7 8 13 14 15 16 17 18 19 22 23 27 28 29 30 32 изиз О Предыдущий ·С ледующий главление 37 37 Принципы включени я антимикр обных препарато в в формул яр лечебнопрофилак тического учрежден ия (IX РНК "Человек и лекарство", Школа для врачей по формулярной системе) © НИИ АХ СГМА 2000, 2001, 2002 Системный кандидоз • В сравнении с 80-ми гг - в 5 раз чаще • В ОИТ: 4 место как возбудитель ангиогенной и 1 место - уроинфекции • Летальность при кандидемии - 25-60% • Антибиотики ШСД - патологическая интестинальная колонизация • Иммуносупрессия - облегчение генерализации – (Б.Р. Гельфанд и соавт., 2000) Патогенез системного кандидоза • Повреждение слизистой ЖКТ (ишемия, ГКС, нарушения метаболизма) • Избыточное размножение Candida spp. в ЖКТ (антибиотики, диабет, травма) • Перитонит, и/абдоминальные абсцессы • Кандидемия • Диссеминированный кандидоз (миокардит (60%), сепсис, ретинит, панофтальмит, менингит, пиелонефрит, пневмония, тромбофлебит и др.) Candida spp. чувствительность к антимикотикам Candida spp. флу Ам В вори каспо albicans +++ +++ +++ +++ glabrata ++ ++ +++ +++ guilliermondii +++ ++ +++ ++ krusei 0 ++ ++ +++ lusitaniae +++ ++ +++ +++ parapsilosis +++ +++ +++ ++ tropicalis +++ +++ +++ +++ Arikan & Rex. Manual of Clinical Microbiology 2003, 8th ed., 1859 +++ высокая активность ++ умеренная активность, отмечена резистентность + низкая активность Антимикотики механизм действия Клеточная мембрана • полиены - АмВ, л-АмВ • азолы - флуконазол - вориконазол Клеточная стенка • ингибиторы синтеза глюкана - каспофунгин Лечение кандидемии вориконазол vs АмВфлуконазол (n=420) вориконазол, n=248 АмBфлу, n=122 100 эффективность (%) NS 80 NS 60 40 41 66 NS 71 41 36 42 20 0 первичный анализ вторичный анализ оценка эффекта только на оценка эффекта на 12 12 неделе наблюдения неделе и на других этапах Kullberg et al. Lancet 2005; 366: 1435-42 летальность Микозы легких в в ХОРИТ кандидоз два варианта – поражение легких при остром диссеминированном кандидозе – аспирационная пневмония наличие Candida spp. в мокроте, БАЛ не является диагностическим критерием инвазивного кандидоза легких, это признак колонизации дыхательных путей диагноз - при выявлении Candida spp. в крови, биоптате и пр. лечение как при других вариантах острого диссеминированного кандидоза Кандидемия, ОДК лечение флуконазол 6-12 мг/кг/сут в/в или п/о амфотерицин В 0,6-1,0 мг/кг/сут в/в вориконазол 6 4 мг/кг/сут в/в или п/о каспофунгин 70 50 мг/cут в/в липидный амфотерицин В 3-5 мг/кг/сут в/в удаление возможных источников инфекции (внутрисосудистых, мочевых катетеров и пр.) Эмпирическая терапия при кандидемии эффективность / время начала лечения (n=134) летальность (%) 40 30 20 10 < 12 12-24 24-48 > 48 Время начала эмпирической терапии после взятия крови на посев, часы Morrell et al., AAC 2005; 49: 3640-45 Эмпирическая фармакотерапия кандидоза • Показания (Брит. о-во АМХ) – Кандидурия у б-х с высоким риском – Однократное выделение С. из крови – Выделение С. из любой стерильной зоны (кроме мочи) – Идентификация грибов из любого биоматериала • С.albicans, C.tropicalis, C.parapsilosis - флуконазол • С.krusei, C.glabrata, C.lusitaniae - амфотерицин • Тяжелая инфекция – сочетание • У беременных – только местно действующие препараты Кандидоз пищевода лечение флуконазол 100-200 мг/сут - 14-28 дней итраконазол по 100-200 мг/сут - 14-28 дней кетоконазол по 200-400 мг/сут - 14-28 дней при резистентности к другим антимикотикам амфотерицин В по 0,3-0,7 мг/кг/сут - 14-28 дней Неабсорбируемые антимикотики (нистатин) неэффективны ! По Н.Н. Климко Системные антимикотики безопасность • Амфотерицин В - нефротоксичность (снижать NaCl) • Кетоконазол, итраконазол гепатотоксичность, снижение секреции стероидов • Флуконазол - токсический потенциал невысок АНТИБАКТЕРИАЛЬНАЯ ТЕРАПИЯ ПРИ ОБОСТРЕНИИ ХОБЛ Простое/неосложнен Осложненное ное обострение обострение ХОБЛ: ХОБЛ: Амоксициллин Макролиды (кларитромицин, азитромицин) Цефалоспорины (цефуроксим и др.) Доксициклин Амоксициллин / клавуланат или «Респираторные» фторхинолоны (левофлоксацин и др.) Азитромицин (при наличии только 1 фактора риска!) Осложненное обострение ХОБЛ (P.aeruginosa): Фторхинолоны с антисинегнойной активностью (ципрофлоксацин, левофлоксацин) Niederman (ERS), 2002; с изме Новые классы/группы антибиотиков, внедренные в практику за последние 10 лет • Оксазолидиноны – Линезолид • Преодоление резистентности Грам + (GISA, VRE) – В перспективе эперезолид, AZD 2563 • Новые фторхинолоны – Левофлоксацин, моксифлоксацин, гатифлоксацин • Повышенная активность против S.pneu, S.aureus • Наиболее высокая у моксифлоксацина (+анаэробы) • По действию на Грам(-) бактерии преимуществ не имеют • Кетолиды (производные 14-членных макролидов) – Телитромицин • Преодоление резистентности S.pneu, БГСА – По действию на Грам(-) преимуществ нет Новые классы/группы антибиотиков, находящиеся на II-III фазе КИ (перспектива 2-3 г) • Липопептиды – Даптомицин • Преодоление резистентности Грам(+) (преим. VRE) • Полусинтетические гликопептиды – Оритаванцин, Далбаванцин • Преодоление резистентности Грам(+), усиление бактерицидности • Глицилциклины – производные миноциклина – Тайгециклин • Широкий спектр – Грам(+) и Грам(-) • Активен против MRSA, PRSP, VRE • Слабая антипсевдомонадная активность Новые классы/группы антибиотиков, проходящие доклинические исследования (5-10 лет) • Карбапенемы – CP 5609 • Анти-MRSA (МПК90 =2) – R-95867 • Дефицит OprD не изменяет МПК для P.aeruginosa • Цефалоспорины ─ LB 11058, TAK-599 • Анти-MRSA (МПК90 = 1-2) Новые мишени • Ингибиторы PDF (пептиддеформилазы) – VCR 3375 • Преимущественная активность против Грам(+) • HARP-антибиотики (Hetero Aromatic Polyamides) • Преимущественно Грам(+) • Ингибиторы эффлюксных насосов – MC-04,124 • Потенцирование эффекта фторхинолонов против P.aeruginosa Задачи микробиологов и клиницистов МИКРОБИОЛОГИ Выделить возбудителя При выделении условно-патогенной микрофлоры определить степень обсеменения Определить антибиотикорезистентность значимого патогена КЛИНИЦИСТЫ Как правильно забрать материал и доставить в нормативные сроки Знать уровни приоритетности возбудителей ГСИ Знать нормобиоз различных локусов организма человека Знать сроки выдачи результатов исследований Уметь интерпретировать результаты микробиологических исследований Наиболее значимые условия достоверности бактериологических исследований Забор материала до начала антибиотикотерапии Соблюдение правил забора и сроков доставки Грамотное оформление сопроводительного документа Эффективное сотрудничество клиницистов и микробиологов Уровень квалификации микробиологов Материально-техническая база лаборатории Правила забора крови 1. В период озноба, температура 37,1-38,5°С 2. Соблюдение правил асептики; наличие спиртовки и помощника 3. Отбор одномоментно в 3 флакона с «двойной средой» 4. Забор достаточного количества крови: 15-20 мл у взрослых, 5-10 мл у детей. 5. Многократно: решает лечащий врач. Митрохин С.Д. Инфекции и антимикробная химиотерапия, 2002. - Т.1 Приказ МЗ РФ № 535 «Об утверждении микробиологических методов исследований …», 1985 FDA категории риска для плода при использовании антимикробных средств А отсутствие риска и отдаленных ______ последствий для плода В С D X нет контролируемых испытаний, Бета-лактамы, подтверждающих риск развития цефалоспорины, фетальных поражений эритромицин, Подтверждена токсичность у животных, риск для человека неопределен Существует риск для плода человека, но польза от применения превышает риск Существует риск для плода человека и нет преимуществ. Противопоказаны у беременных азитромицин Хлорамфеникол, ФХ кларитромицин, ванкомицин, гентамицин, бисептол Тетрациклин, аминогликозиды ________ Антибиотики у беременных • Средняя частота назначения – 12% • Реальный риск для плода?? – Олеандомицин – незрелость – Кларитромицин – спонтанные аборты – Триметоприм – дефекты ССС • Теоретический риск – С: фторхинолоны, ванкомицин, гентамицин, имипенем – D: тетрациклин, другие аминогликозиды – Х: нет Чилова Р.Я. И соавт, 2005 Слайд Слайд 532 7 8 13 14 15 16 17 18 19 22 23 27 28 29 30 изиз О Предыдущий ·С ледующий главление 37 37 Принципы включени я антимикр обных препарато в в формул яр лечебнопрофилак тического учрежден ия (IX РНК "Человек и лекарство", Школа для врачей по формулярной системе) © НИИ АХ СГМА 2000, 2001, 2002