9 класс.химия. Вводная контрольная работа 1docx
реклама

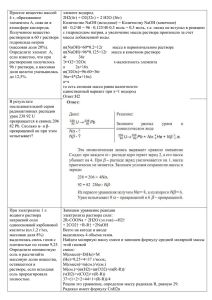
9 класс. Химия. Вводная контрольная работа за курс 8 класс. 1 вариант. Часть «А». Дать короткий ответ. Из предложенного списка сложных веществ выписать: : MgO, H2SO3, SO2, HCl, BaO, NaOH, Al2O3, Al (OH)3, N2O5, HJ, NaNO3, HBr, HMnO4, Zn(OH)2, HNO3, LiOH, Ba(OH)2, CaCO3, Mn2O7, Li2O 1) 2) 3) 4) Основные оксиды Растворимые основания Кислоты Соли Часть «Б». Закончить возможные уравнения реакций: 5) BaCl2 + H2SO4 > CuSO4 + H2S > AlCl3 + NaOH > CrCl3 + KOH > Ca(NO3)2 + Na3PO4> LiCl + Pb(NO3)3 > 6) Осуществить превращение: Zn > ZnO > ZnCl2 > Zn(OH)2 > ZnSO4 Часть «В». На вычисление молярной массы и массовой доли вещества: 7) А) Определить М.М. и массовую долю KMnO4 Б) Fe3O4 8) Используя формулу: M= m\v (г\моль), расчитайте и запишите ответ А) Какое количество вещества содержится в образце алюминия массой 10,8 гр. Б) Определить массу 2 моль железа. Ответы и критерий оценок: Часть «А». За каждый правильный ответ 1 балл. Всего 11 1) 2) 3) 4) баллов. Основные оксиды: MgO, BaO. Растворимые основания: NaOH, Ba (OH)2, LiOH Кислоты: H2SO3, HCl, HBr, HMnO4, HNO3. Соли: NaNO3 Часть «Б». За каждое, правильное решенное уравнение реакции 2 балла. Всего 20 баллов. 5) BaCl2 + H2SO4 > BaSO4 + 2HCl. 3NaOH > Al (OH)3 + 3NaCl, CuSO4 + H2S > не идет, AlCl3 + CrCl3 + 3KOH > Cr (OH)3 + 3KCl, 3Ca(NO3)2 +2 Na3PO4> Ca3 (PO4)2 + 6NaNO3, 3 LiCl + Pb(NO3)3 > PbCl3 +3 LiNO3 6) Осуществить превращение: Zn > ZnO > ZnCl2 > Zn(OH)2 > ZnSO4 2Zn + O2> 2ZnO, ZnO + HCl > ZnCl2 + H2O, Zn Cl2 +2 NaOH > Zn (OH)2 + 2NaCl, Zn (OH)2 + H2SO4 > ZnSO4 + 2H2O Часть «В». За каждое правильное решение 2 балл. Всего 8. 7) А) Определить М.М. и массовую долю KMnO4. М.м =158. W (K)=25% Mn=35%, O= 40% Б) Fe3O4. M/m= 232 W (Fe)=72 %, W (O)=28 % 8) Используя формулу: M= m\v (г\моль), расчитайте и запишите ответ А) Какое количество вещества содержится в образце алюминия массой 10,8 гр. V= 10,8\ 27=0,4 моль Б) Определить массу 2 моль железа. M= 2*56= 112 г\моль. Итого 40 баллов: менее 20 «2», 21 – 26 «3», 27 – 33 «4», более 34 «5».