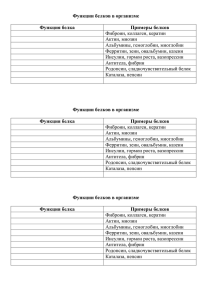
Тема: Органические вещества клетки. Белки Цель урока
реклама
Тема: Органические вещества клетки. Белки Цель урока Задачи Средства обучения Тип урока: Метод проведения Ученик должен Ход урока. Сформировать представления об уникальных особенностях строения молекул белков, расширить знания о важнейшей роли в жизнедеятельности живых организмов на основе изучения свойств и функций белков. образовательная: показать взаимосвязь строения и выполняемой функции на примере белков, входящих в состав клетки; развивающая: продолжать формировать умения: выделять главное, анализировать, устанавливать причинноследственную связь. таблицы «Строение белков», «Функции белков», мультимедийное приложение к учебнику «Биология. Общие закономарности.9 класс» комбинированный Лекция с использованием опорных конспектов иметь представление о структурной организации молекул белков; знать особенности строения молекул белков; основные функции белков; уметь объяснять значение белков. I.Организационный момент. II.Актуализация, мотивация и целеполагание. Вспомните определения «жизни», данные Ф. Энгельсом и Волькенштейном. Что можно сказать о роли белков на основании этих определений? Сформулируйте цель урока, прочитав названия пунктов параграфа §2.5 (может вызвать затруднение в формулировке цели « …изучить свойства белков» пункт «Денатурация и ренатурация белков») III.Проверка знаний и умений. 1.Работа с терминами (дать устно определение, «Цепочка», один учащий дает определение, другой иллюстрирует сказанное примерами): органические вещества, полимеры, мономеры, гомополимеры гетерополимеры, липиды, углеводы, моносахариды, дисахариды, полисахариды. 2.Беседа по вопросам: Охарактеризуйте содержание углеводов в клетках различных живых организмов. В учебнике на стр. 42 в рамке Функции простых и сложных углеводов. Метод свободного выбора : работа с текстом учебника на стр.41-42 или заполнение кластера. IV. Изучение нового материала. 1. Белки — азотсодержащие органические соединения, макромолекулы, гетерополимеры, мономером является аминокислота. Запись на доске NH2-CH-COOH R где NH 2 – аминогруппа (основные свойства) СООН-карбоксильная группа (кислотные свойства) R –радикал В состав белков входят 20 аминокислот. заменимые синтезируются в организме незаменимые не могут быть синтезированы в организме человека и животных, должны поступать с пищей (арг, гис, три, мет, лиз, вал, лей, илей, тре) В зависимости от R неполярные полярные незаряженные ала, вал, лей, илей, про, мет, фен, три гли, сер, тре, цис, тир, асн, глн полярные заряженные + лиз, арг, гис асп, глу Запись на доске Специфичная последовательность чередования аминокислот в белке определяется генетически. Аминогруппа одной аминокислоты способна вступать в реакцию с карбоксильной группой другой аминокислоты с образованием дипептида посредством пептидной связи (C—N). Если соединяется много аминокислот (более 10), то получается полипептид. 2. Структуры белковой молекулы. Первичная, вторичная, третичная, четвертичная структуры белковых молекул, формирующиеся на основе различных химических связей внутри и между молекулами. ( И н ф о р м а ц и я у ч и т е л я с и с п о л ь з о в а н и е м т а б л и ц ы «Уровни организации белка»). Таблица «Уровни организации белка» Просмотр фрагмента мультимедийного приложения к учебнику 9 класса с целью изучения свойств белков. 1. Первичная структура (линейная) полипептид, связанный пептидными связями (связь C-N, между карбоксильной группой одной аминокислоты и аминогруппой другой аминокислоты). Специфична, определяется последовательностью нуклеотидов ДНК, кодирующей данный белок. 2. Вторичная структура а-спираль (пружина), β-слой (складчатый слой): водородные связи (связь между H аминогруппы и О карбоксильной группы). Кератин (а-спираль), фиброин (р-слой). 3. Третичная структура - суперспираль, глобула: связи междy радикалами: дисульфидные (S-S связи), ионные, водородныеl, гидрофобные взаимодействия. Инсулин. 4. Четвертичная структура – несколько третичных структур:слабые взаимодействия между радикалами и Ван-дер-Ваальсовы силы между субъединицами. Гемоглобин (2а и 2β -цепи), лактатдегидрогеназа, миозин. Денатурация - утрата конформации, присущей данной белковой молекуле. Денатурацию вызывают: нагревание, воздействие излучений, сильные кислоты, щелочи, концентрированные растворы солей, тяжелые Me, органические растворители, детергенты. Если сохраняется первичная структура белка, то возможна ренатурация, то есть восстановление конформации белка. 3.Классификация белков. Белки по структуре: Фибриллярные(вторичная структура, не растворимы в воде, механическая прочность-коллаген, миозин, кератин Глобулярные (третичная структура, растворимы в воде – антитела, ферменты, гормоны Промежуточные (фибриллярные, но растворимы в воде – фибриноген) Белки по составу сложные (протеиды) состоят из простые (протеины) состоят аминокислот только из аминокислот и небелковой части (простетической группы) альбумины, глобулины, гистоны, актин, фосфопротеиды (казеин молока, миозин, фибриноген, пищеварительные пепсин), гликопротеиды (мугщн), ферменты металлопротеиды (ферритин), нуклеоптротеиды (в составе ДНК, РНК), липопротеиды (компоненты мембран), хромопротеиды (гемоглобин) 4.Динамическая пауза. Опорный конспект проецируется на доску. 5. Функции белков. Самостоятельная работа с текстом §2.5 с целью нахождения фактов, подтверждающих данные опорного конспекта. Ответы учащихся с дополнениями учителя. 1. Структурная: клеточные мембраны органоидов клеток и внеклеточных структур; кератин (волосы), фиброин (шелк), коллаген (хрящ, сухожилия), эластин (связки). 2. Двигательная: сократительные белки — актин (неподвижные нити миофибриллы) и миозин (подвижные нити миофибриллы). 3. Транспортная: гемоглобин (транспорт О2 и СО2 в крови), трансферрин (транспорт железа), миоглобин (транспорт O2 в мышцах). 4. Защитная: антитела (иммуноглобулины), фибриноген, тромбин. 5. Регуляторная: гормоны инсулин, глюкагон, АКТГ, соматотропин. 6. Рецепторная: в составе мембранных рецепторов обеспечивают ответ клетки на раздражение (родопсин). 7. Запасающая: резервные источники энергии: яичный альбумин, казеин молока. 8. Энергетическая (в самую последнюю очередь): при расщеплении 1 г белка выделяется 17,6 кДж энергии. 9. Токсины (змеиный яд, дифтерийный токсин), антибиотики (неокарциностатин). 10. Каталитическая: белки-ферменты биологические катализаторы, то есть вещества, ускоряющие реакции. Их свойства: все ферменты - глобулярные белки (искл. рибозим - РНКфермент); увеличивают скорость реакции, но сами не расходуются; активность меняется в зависимости от t°, рН, давления, концентрации; обладают специфичностью, то есть один фермент катализирует только одну реакцию. V. Закрепление знаний. VI. Домашнее задание. VI. РефлексияI Выполнение заданий № 10,11,13 в рабочей тетради на стр.37-38 с предварительным обсуждением алгоритма действий. Изучить текст §2.5, отвечать на вопросы после параграфа, в рабочей тетради на стр.38 № 15 выполнить письменно. Оценивание работы учащихся этапов урока (5 –все понравилось, не устал; 4интересно, немного устал;3 –было сложно, устал; 2-совсем не интересно, не устал; 1-совсем не интересно, устал.)