Сравнительная оценка морфологических изменений
реклама

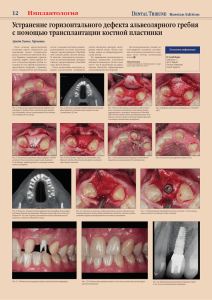
УДК 616. 716. 8 – 018. 4 – 089. 843 – 092. 4 СРАВНИТЕЛЬНАЯ ОЦЕНКА МОРФОЛОГИЧЕСКИХ ИЗМЕНЕНИЙ ОСТЕОИНТЕГРАЦИИ В ДИНАМИКЕ ПРИМЕНЕНИЯ РАЗЛИЧНЫХ ЛЕЧЕБНЫХ КОМПЛЕКСОВ В УСЛОВИЯХ ЭКСПЕРИМЕНТА И.О. Походенько-Чудакова, Л.А. Пашкевич, Т.Л. Шевела УО «Белорусский государственный медицинский университет (ректор к.м.н., доцент А.В. Сикорский), ГУ «Республиканский научно-практический центр травматологии и ортопедии» (директор д.м.н., профессор Заслуженный деятель науки Республики Беларусь А.В. Белецкий), Белорусский Сотрудничающий Центр Европейской Ассоциации черепно-челюстно-лицевой хирургии (директор центра д.м.н., профессор, Заслуженный деятель науки Республики Беларусь О.П. Чудаков) Цель работы – провести сравнительную оценку морфологических изменений остеоинтеграции в системе челюсть – дентальный имплантат в динамике применения различных лечебных комплексов в условиях эксперимента. Исследование выполнено на 69 кроликах. Серию 1 (21 животное), которая дополнительного лечения не получала. Данная серия была контрольной. Серия 2 (48 животных), которой проводили курс иглоукалывания. Забор материала для патогистологического исследования осуществляли в сроки на 3, 7, 14, 21 сутки и через 1, 2, 6 месяцев после операции. Результаты доказывают, что использование рефлексотерапии в послеоперационном периоде при дентальной имплантации создаёт наиболее благоприятные условия для течения процессов остеоинтеграции в системе челюсть – дентальный имплантат. Ключевые слова: дентальная имплантация, остеоинтеграция, рефлексотерапия, морфологические изменения. Введение. В течение последних десятилетий метод дентальной имплантации занял достойное место среди других видов специализированной помощи, оказываемой челюстно-лицевыми хирургами и стоматологами-ортопедами. [8, 14]. Конструкции имплантатов и техника оперативных вмешательств по их постановке постоянно совершенствуется и обновляется. Важным для каждой из подобных разработок является обеспечение стабильности процессов остеоинтеграции в системе челюсть – дентальный имплантат [4, 7, 11]. Даже при технически правильно выполненной операции и адекватном протезировании, такие факторы как особенности анатомо-физиологических условий полости рта, значительные жевательные нагрузки на имплантат способны привести к нарушению процесса взаимодействия с ним костной ткани. Успех имплантации определяется правильностью определения показаний к выполнению дентальной имплантации, выбора конструкции имплантата, адекватной конкретной клинической ситуации, техники проведения операции и послеоперационной реабилитации. Современное представление об остеоинтеграции дентальных имплантатов выведено в стройную концепцию морфологического обоснования их использования на основании данных адаптации определение указывающее костной ткани к имплантату P. Branemark (1993) дает что, «остеоинтеграция есть прямая структурная и функциональная связь между упорядоченной живой костью и поверхностью несущего нагрузку имплантата» [10]. Рассматриваемый процесс обеспечивает структурное и функциональное соединение живой кости с поверхностью имплантата. Репаративная регенерация костной ткани как биологический процесс является генетически предрасположенным, его нельзя ускорить. Однако существуют факторы регенерации, на которые можно оказывать оптимизирующее воздействие. При операции дентальной имплантации они приобретают особую значимость, следовательно, возрастает роль средств, обладающих оптимизирующим действием на остеогенез. Известны публикации, свидетельствующие о позитивном влиянии рефлексотерапии на репаративную регенерацию костной ткани вообще [5, 9, 13] и челюстных костей в частности [6]. Изложенный материал убеждает в том, что изучение влияния рефлексотерапии на процессы остеоинтеграции в системе челюсть - дентальный имплантат является актуальным и целесообразным. Цель работы – провести сравнительную оценку морфологических изменений остеоинтеграции в системе челюсть – дентальный имплантат в динамике применения различных лечебных комплексов в условиях эксперимента. Объекты и методы. Исследование выполнено на 69 самцах кроликов породы Шиншилла одного возраста и массы тела. Экспериментальные исследования выполняли в строгом соответствии экспериментальными с животными. требованиями, При регламентирующими проведении инвазивных работу процедур с были использованы стандарты American Heart Association`s «Guidelines for the Use of Animal in Reserch» и Guide for the core and Use of Laboratory Animals (National Academy Press, Revised, 1996) [1]. Экспериментальным животным под внутривенным наркозом были выполнены операции удаления правого центрального нижнего резца с последующей непосредственной дентальной имплантацией с использованием имплантатов системы «Верлайн». После операции однократно внутримышечно кроликам вводили 500000 ЕД бензилпенициллина с целью профилактики развития гнойно-воспалительных осложнений. Указанные экспериментальные животные были разделены на две серии. Серию 1 составило 21 животное, которым дополнительных лечебно-реабилитационных мероприятий не проводили. Данная серия являлась контрольной. Серия 2 (основная) включала 48 животных, которым в течение 10 дней выполняли курс иглоукалывания. Раздражение наносили сильным тормозным методом с экспозицией 30 минут на акупунктурную точку аналогичную GI4, определявшуюся в соответствии с данными специальной литературы [2, 12]. В сроки на 3, 7, 14, 21сутки и 1, 2, 6 месяцев животных выводили из эксперимента, и осуществляли забор материала для патогистологического исследования. Выпиливание блоков нижней челюсти кроликов проводили, отступя 0,5-0,7 см по обе стороны от ложа имплантата. Материал фиксировали в 10% растворе нейтрального формалина, подвергали декальцинации в азотной кислоте, проводили по стандартной схеме через спирты восходящей крепости и заключали в парафин [3]. Изготовленные серийные гистологические срезы окрашивали гематоксилином и эозином с последующим заключением в бальзам. Гистологические препараты подвергли тщательному изучению с использованием световой микроскопии. Результаты. Патогистологическое изучение микропрепаратов и сравнительная оценка морфологических изменений остеоинтеграции в системе челюсть – дентальный имплантат в динамике применения различных лечебных комплексов в условиях эксперимента позволили констатировать следующее. В серии контроля на 3-и сутки после операции по краям имплантационной полости выявлялись в основном некробиотические и некротические изменения костной ткани, которые выражались в неоднородности окраски, некрозе части остеоцитов, а также тканей межбалочных пространств. Встречались крупно- и мелкоочаговые кровоизлияния. Стенка полости представлена рыхлой тканью с мелко- и крупноочаговыми скоплениями эритроцитов. При этом же сроке наблюдения в основной серии наряду с некротическими и некробиотическими изменениями в костных тканях имплантационной полости отмечается начало пролиферативных процессов по краям материнской кости с образованием нежноволокнистой грануляционной ткани с крупно- и мелкоочаговыми скоплениями эритроцитов. В отдельных полях зрения просматриваются небольшие скопления «сочных» остеобластов, продуцирующих остеоидное вещество розового цвета (рис. 1). На 7-ые сутки в препаратах контрольной серии определялась незначительной ширины соединительнотканная прослойка между имплантатом и материнской костью. В поверхностных участках кости, отграничивающих имплантационную полость просматривается мелкопетлистая сеть вновь образованных коллагеновых волокон с небольшими вкраплениями остеоидного вещества. Со стороны материнской кости имеются безостеоцитные участки. Отмечается пазушная и остеокластическая резорбция. В тоже время в основной серии наблюдения обращало на себя внимание истончение кортикального слоя кости в области имплантационного ложа. Костная ткань имела компактное строение, местами отмечалась рарефикация. Кое-где по краям просматривались безостеоцитные участки. Между ложем имплантата и костью имелся широкий слой соединительной ткани. В месте непосредственного контакта с имплантатом пучки коллагеновых волокон имели параллельную ориентацию. По направлению к периферии волокнистая соединительная ткань носила более зрелый характер, становилась грубоволокнистой, менее клеточной и васкуляризированной. Встречались очаговые скопления лимфоидных клеток и макрофагов. Местами на костный край материнской кости напластовывалось вновь образованное остеоидное вещество. В этот же срок наблюдения в основной серии определялась незначительной ширины соединительнотканная прослойка между имплантатом и материнской костью. В поверхностных участках кости, отграничивающих имплантационную полость просматривается мелкопетлистая сеть вновь образованных коллагеновых волокон с небольшими вкраплениями остеоидного вещества. Со стороны материнской кости имеются безостеоцитные участки. Отмечается пазушная и остеокластическая резорбция. К 14-ым суткам в серии контроля по краям имплантационной полости заметно истончение кортикальной костной пластинки. Костная ткань имела пластинчатое компактное строение с участками рарефикации. По самому краю материнской кости ложа просматривались безостеоцитные участки кости. К последнему плотно прилегал пласт соединительной ткани, переходящей в направлении к имплантату в клеточноволокнистую соединительную ткань с параллельно расположенными пучками коллагеновых волокон. В отдельных полях зрения соединительная ткань была более зрелой, плотной, приобретала более грубоволокнистое строение, уменьшалось количество клеточных элементов, терялась их «сочность». Они приобретали более вытянутую форму. Снижалась васкуляризация. В 2-х наблюдениях отмечались скопления лимфомакрофагальных клеточных элементов. Местами на костный край материнской кости происходило напластование вновь образованных остеоидных структур. В препаратах основной серии к 14-ым суткам наблюдений по краю имплантационной полости со стороны материнской кости заметна активизация костеобразовательных процессов. Наряду с полями недифференцированного остеоидного матрикса с «сочными» остеобластическими клеточными элементами просматриваются густая сеть сетчатоволокнистой и параллельноволокнистой остеоидной ткани. На 21-ые сутки в контрольной серии в материнской кости имплантационного ложа просматривались безостеоцитные участки кости. Кое-где встречались остеокласты в гаупшиповых лакунах. По поверхности полости имелся широкий слой грубоволокнистой соединительнотканной прослойки зрелого вида с небольшим количеством вытянутых фибробластических клеточных элементов, со слабо выраженной васкуляризацией. Кое-где видны были скопления лимфомакрофагов. В единичных участках по краям материнской кости имелись остеоидные структуры мелкопетлистого вида. В этот же срок наблюдения в препаратах основной серии реже встречаются безостеоцитные участки в материнской кости. Не выявляется резорбции костного вещества. По краям хорошо различима густая сеть вновь образованных костных балочек различной степени зрелости, окружённых цепочкой «возбуждённых», «сочных» остеобластических клеточных элементов. Межбалочные пространства выполнены фиброретикулярной клеточной тканью (рис. 2). Через 1 месяц в серии контроля в костной стенке имплантационного ложа продолжает наблюдаться остеокластическая резорбция костного вещества. По краю материнской кости отмечается лизис костных клеточных элементов, к ней вплотную прилежит слой грубоволокнистой зрелой соединительной ткани, бедной клеточными элементами. Местами просматриваются поля остеоидной и слабо обызвествлённой ткани, имеющий иррегулярное строение грубоволокнистого характера. В указанный срок наблюдения в основной серии препаратов полость окружена густой сетью вновь образованных костных балочек трабекулярного строения. Местами граница между материнской костью и вновь образованной костной тканью со стороны имплантационной полости с трудом различима. Через 2 месяца наблюдений препараты основной серии отличало то, что была видна сеть костных структур тесно спаянных с материнской костью имплантационного ложа. Продолжаются процессы вторичной перестройки образовавшихся костных структур на зрелые, функционально адаптированные. При сроке наблюдения 6 месяцев в препаратах контрольной серии по краю материнской кости имплантационного ложа просматривалась различной ширины соединительнотканная прослойка с крупнопетлистой сетью новообразованных остеоидных и слабообызвествлённых костных структур. В подлежащей материнской кости отмечались остеолитические процессы по типу пазушной и остеокластической резорбции. В основной серии при данном сроке наблюдения граница между вновь образованной и материнской костью практически неразличима. Во вновь образованных структурах завершаются процессы вторичной перестройки новообразованной кости на функционально детерминированные зрелые костные структуры (рис. 3). Таким образом, при сравнительном сопоставлении патоморфологического изучения препаратов контрольной и основной серий следует отметить, что в серии 2 во все сроки наблюдения отмечено более быстрое, чем в контроле созревание клеточно-волокнистых структур соединительнотканной прослойки между имплантатом и материнской костью. Также следует подчеркнуть, что в основной серии в значительно меньшей степени выражены проявления некроза и некробиотоза остеоцитов по краю материнской кости. Края её имели более ровный и мене зазубренный вид. Резорбтивные изменения выявлялись в ранние сроки и были незначительными уже к концу 1-го месяца наблюдений. Более интенсивное развитие костеобразовательных процессов в области имплантации также было отмечено в основной серии. По краям имплантационной полости более активно и в более ранние сроки формировались мелко- и крупнопетлистые структуры из вновь образованного остеоидного вещества. Процессы вторичной перестройки вновь образованного костного вещества в серии 2 начинались в более ранние сроки и были заметны уже в стадии формирования остеоидного матрикса, что выражается в образовании молодой мелкопетлистой костной ткани среди полей недифференцированного костного матрикса. Заключение. Приведенные данные доказывают, что использование рефлексотерапии в послеоперационном периоде при дентальной имплантации создаёт наиболее благоприятные условия для течения процессов остеоинтеграции в системе челюсть – дентальный имплантат. Литература. 1. Денисов, С.Д. Требования к научному эксперименту с использованием животных / С.Д. Денисов, Т.С. Морозкина // Здравоохранение. - 2001. - № 4. - С. 40–42. 2. Казеев, Г.В. Ветеринарная акупунктура / Г.В. Казеев. - М.: РИО РГАЗУ, 2000. – 398 с. 3. Корж, А.А. Репаративная регенерация кости / А.А. Корж, А.М. Белоус, Е.Я. Панков М.: Медицина, 1972. - 232 с. 4. Никольский, В.Ю. Внутрикостная дентальная имплантация / В.Ю. Никольский. – Самара: СамГМУ, 2004. – 40 с. 5. Полякова, А.Г. Восстановительное лечение больных травматолого-ортопедического профиля с использованием рефлексотерапии: автореф. дис. … канд. мед. наук: 14.00.22 / А.Г. Полякова; НИИТиО им. В.В.Вредена. - Л., 1989. - 20 с. 6. Походенько-Чудакова, И.О. Влияние акупунктуры на регенерацию травматических повреждений костной ткани нижней челюсти в эксперименте / И.О. ПоходенькоЧудакова, С.Д. Беззубик // Сборник науч. статей Республ. научн.-практ. конф. «Актуальные проблемы медицины», 15-й науч. сессии ГГМУ, посвящ. 60-летию Победы в Великой Отечественной войне. Гомель: УО ГГМУ, 2005. – Т. 3. - Вып. 6. - С. 89–90. 7. Применение дентальных имплантатов спиралевидной формы у больных с дефектами зубных рядов: учеб.-метод. пособие / И.М. Байриков [и др.]. – Самара: ООО «БМВ и К», 2010. – 24 с. 8. Робустова, Т.Г. Имплантация зубов (хирургические аспекты) / Т.Г. Робустова. – М.: Медицина, 2003. - 560 с. 9. Системы комплексной электормагнитотерапии / А.М. Беркутов [и др.]. - М: Лаборатория базовых знаний, 2000. - 376 с. 10. Branemark, P. Osseointegration and its experimental background / P.-I. Branemark // J. Pros. Dent. – 1993. – Vol. 50. – P. 399-412. 11. Evalution of the difference in accuracy between implant placement by virtual planning data and surgical guide templates versus the conventional free-hand method – a combined in vivo – in vitro technique using cone-beam CT (Part II) / H.J. Nickenig [et al.] // J.Cranio-maxilloFacial Surgery. – 2010. – Vol. 38, № 7. – P. 488-493. 12. Lee, Chunzhen. Experimental chen-tzu / Chunzhen Lee. – Beijing: Chinese pharmacological publishing house, 2004. – 253 p. 13. List, T. Acupuncture and occlusal splint therapy in the treatment of craniomandibular disorders II. A 1-year follow-up study / T. List, M. Helkimo // Acta Odontol. Scand. - 1992. Vol. 50, № 6. - P. 375-385. 14. Sakka, S. Simultaneous maxillary sinus lifting and implant placement with autogenous parietal bone graft: Outcome of 17 cases / S. Sakka, Ch. Krenkel // J.Cranio-maxillo-Facial Surgery. – 2011. – Vol. 39, № 3. – P. 187-191. а б Рис. 1 Микрофото. Сравнительная оценка морфологических изменений остеоинтеграции в системе челюсть – дентальный имплантат в динамике применения различных лечебных комплексов на 3-и сутки наблюдения: а – серия контроля: клеточно-волокнистая ткань выстилающая имплантационную полость с мелко- и крупноочаговыми скоплениями эритроцитов. Окраска гематоксилином и эозином. x 400; б – основная серия: видна грануляционная ткань, скопление эритроцитов, остеоидное вещество. Окраска гематоксилином и эозином. x 100. а б Рис. 2 Микрофото. Сравнительная оценка морфологических изменений остеоинтеграции в системе челюсть – дентальный имплантат в динамике применения различных лечебных комплексов на 21-ые сутки наблюдения: а – серия контроля: видны остеоидные структуры у края материнской кости. Окраска гематоксилином и эозином. x 200; б – основная серия: видна густая сеть вновь образованных слабообизвествлённых балочек. Окраска гематоксилином и эозином. x 100. а б Рис. 3 Микрофото. Сравнительная оценка морфологических изменений остеоинтеграции в системе челюсть – дентальный имплантат в динамике применения различных лечебных комплексов через 6 месяцев наблюдения: а – серия контроля: видны вновь образованные остеоидные структуры по краю материнской кости. Окраска гематоксилином и эозином. x 200; б – основная серия: граница между материнской и вновь образованной костью практически неразличима, видны линии склеивания. Окраска гематоксилином и эозином. x 200.