Компьютерный поиск потенциальных ингибиторов 15
реклама

Башкирский государственный университет, г.Уфа
кафедра физической химии и химической экологии
____________________________________________________________________________________
Компьютерное моделирование
взаимосвязи «структура-свойство»
в ряду азот-, кислород- и
серусодержащих ингибиторов
биосинтеза лейкотриенов и
блокаторов чувствительных к ним
рецепторов
Хайруллина Вероника Радиевна
Научный консультант: д.х.н., проф. Герчиков А.Я.
Характеристика биологического действия основных типов эйкозаноидов
Эйкозаноид
PG E2
PG F2α
PG D3
PG I2
TX A2
TX A3
LT B4
Группа
лейкотриенов
LTC4→
LT D4→
LTE4→
LXA4
Основное место
Основное биологическое действие
синтеза
Большинство тканей, Расслабляет гладкую мускулатуру, расширяет сосуды,
особенно почки
инициирует родовую активность, подавляет миграцию
лимфоцитов, пролиферацию Т-клеток.
Большинство тканей Сокращает гладкую мускулатуру, суживает сосуды, бронхи,
стимулирует сокращения матки.
Клетки гладкой
Вызывает расширение сосудов, снижает агрегацию тромбоцитов
мускулатуры
и лейкоцитов.
Сердце, клетки
Уменьшает агрегацию тромбоцитов, расширяет сосуды. В
эндотелия сосудов
клетках-мишенях увеличивает образование цАМФ.
Тромбоциты
Стимулирует агрегацию тромбоцитов, суживает сосуды и
бронхи, в клетках уменьшает образование цАМФ.
Тромбоциты
Обладает функциями, одинаковыми с ТХ А2, но значительно
менее эффективен.
Клетки белой крови, Стимулирует хемотаксис и агрегацию лейкоцитов, освобождение
клетки эпителия
лизосомальных ферментов лейкоцитов. Увеличивает
проницаемость сосудов.
Клетки белой крови, Стимулируют расширение сосудов, увеличивают их
альвеолярные
проницаемость. Вызывают сокращение бронхов.
макрофаги
Основные компоненты «медленно реагирующей
субстанции» анафилаксии.
Лейкоциты
Активирует хемотаксис и стимулирует образование супероксид
аниона в лейкоцитах.
Механизм окисления арахидоновой
кислоты под действием 5-липоксигеназы
2
Цель: Изучение взаимосвязи «структура – активность» в ряду
эффективных ингибиторов образования лейкотриенов и
чувствительных к ним рецепторов.
Задачи:
• Изучение структурных закономерностей в ряду эффективных
ингибиторов каталитической активности изомерных форм
липоксигеназ (5/15-ЛОГ), а также лейкотриен А4-гидролазы.
Построение математических моделей прогноза и распознавания
эффективных ингибиторов данных рецепторов
• Изучение структурных закономерностей в ряду эффективных
блокаторов рецепторов BLT1 и BLT2. Построение математической
модели прогноза и распознавания эффективных блокаторов
рецепторов BLT1 и BLT2.
• Молекулярный дизайн потенциально эффективных ингибиторов
образования лейкотриенов.
3
Основные этапы расчетов в ИС SARD–21 (Structure Activity Relationship & Design)
Формирование обучающей и экзаменационной выборки
Дезагрегирование структур обучающей выборки и
формирование субструктурных дескрипторов
Оценка характера влияния дескрипторов на активность
Формирование решающего набора признаков (РНП)
Тестирование РНП на структурах обучающей и
экзаменационной выборок
Выбор направлений молекулярного дизайна
МОДИФИКАЦИЯ СТРУКТУР ПО
ВЫБРАННЫМ НАПРАВЛЕНИЯМ
ЭКЗАМЕН СОЕДИНЕНИЙ И ОТБОР ЛУЧШИХ
4
Расчет коэффициента информативности
структурных признаков в рамках системы
SARD-21
Коэффициент
информативность признаков r
вычисляется по формуле
Пример:
А-активные
В-неактивные
n1 n4 n2 n3
r
( N1 N 2 N 3 N 4)1/ 2
N1=20 структур
N2=20 структур
-1 ≤ r ≤ +1
n1=5
n3=2
где n1 и n2 – число структур
группы А, содержащих и не
содержащих данный фрагмент
n3 и n4 – то же для группы В
N1 и N2 – число структур в
группах А и В
N3=n1+n3,
N4=n2+n4
n2=15
n4=18
фрагмент (–СН2-ОН)
N3=n1+n3=5+2=7
N4=n2+n4=15+18=33
5 18 15 2
r
0,197
1/ 2
(20 20 7 33)
5
Характеристики моделей
Модель М1 прогноза
ингибирующей
активности
в отношении
5-липоксигеназы
клеток крови крыс
(ВЭС+СЭС/НЭС)
Модель М2 прогноза
ингибирующей
активности
в отношении
5-липоксигеназы
клеток крови крыс
(ВЭС/СЭС+НЭС)
Модель М3 прогноза
ингибирующей
активности
в отношении
5-липоксигеназы
клеток крови человека
(ВЭС/СЭС+НЭС)
Модель М4 прогноза
ингибирующей
активности
в отношении
5-липоксигеназы
клеток крови человека
(ВЭС+СЭС/НЭС)
Ряд А – 51 структура
со средней ингибирующей
активностью,
IC50< 5 мкмоль/л
Ряд В – 40 структуры
с низкой
ингибирующей
активностью
IC50> 7 мкмоль/л
Ряд А – 50 структур
с высокой
ингибирующей
активностью
IC50< 1.5 мкмоль/л
Ряд В – 48 структуры
с средней ингибурующей
активностью
IC50> 2.5 мкмоль/л
Ряд А – 93 структуры
с средней ингибирующей
активностью,
IC50< 3 мкмоль/л
Ряд В – 82 структуры
с низкой
ингибирующей
активностью
IC50> 5 мкмоль/л
Ряд А – 85 структур
с высокой
ингибирующей
активностью
IC50< 3,2 мкмоль/л
Ряд В – 72 структуры
с средней ингибурующей
активностью
IC50> 7,7 мкмоль/л
Экзаменационная
выборка – 25 структур
Экзаменационная
выборка – 25 структур
Экзаменационная
выборка – 29 структур
Экзаменационная
выборка – 29 структур
6
Характеристики моделей
лейкотриен А4-гидролаза
Модель М5 прогноза
Модель М6 прогноза
ингибирующей
ингибирующей
активности
активности
в отношении
в отношении
лейкотриен А4-гидролазы* лейкотриен А4-гидролазы*
(ВЭС/СЭС+НЭС)
(ВЭС+СЭС/НЭС)
Ряд А – 108 структур
с высокой ингибирующей
активностью,
IC50< 1 мкмоль/л
Ряд В – 84 структуры
со средней
ингибирующей
активностью
IC50> 2 мкмоль/л
Ряд А – 57 структур
со средней
ингибирующей
активностью
IC50< 5 мкмоль/л
Ряд В – 44 структуры
с низкой ингибурующей
активностью
IC50> 10 мкмоль/л
Экзаменационная
выборка – 30 структур
Экзаменационная
выборка – 30 структур
*метод связывания
рецептора из
полиморфонуклиарных
*метод связывания
рецептора из
полиморфонуклиарных
клеток с радиолигандом
клеток с радиолигандом
антогонисты BLT1 и BLT2
Модель М7 прогноза
антогонистической
активности в
отношении BLT1 и BLT2
по функциональной
активности*
(ВЭС/СЭС+НЭС)
Модель М8 прогноза
антогонистической
активности в
отношении BLT1 и BLT2
по методу связывания*
(ВЭС/СЭС+НЭС)
Ряд А – 44 структур
с высокой
антогонистической
активностью
IC50< 1 мкмоль/л
Ряд В – 43 структур
со средней
антогонистической
активностью
IC50> 1 мкмоль/л
Ряд А – 81 структур
с высокой
антогонистической
активностью
IC50< 1 мкмоль/л
Ряд В – 48 структур
со средней
антогонистической
активностью
IC50> 1 мкмоль/л
Экзаменационная
выборка – 26 структур
Экзаменационная
выборка – 27 структур
*хемотаксис
изолированных
нейтрофилов человека
*метод связывания
рецептора из
полиморфонуклиарных
клеток с радиолигандом
7
Характеристики моделей
Ингибиторы 15-ЛОГ
Модель М9 прогноза
ингибирующей
активности
в отношении
15-липоксигеназы
ретикулоцитов диких кроликов
(ВЭС+СЭС/НЭС)
Ряд А – 57 структур
с высокой и средней
ингибирующей
активностью,
IC50< 10 мкмоль/л
Ряд В – 46 структур
с низкой
ингибирующей
активностью
IC50> 100 мкмоль/л
Экзаменационная
выборка – 36 структур
*метод связывания
рецептора из
полиморфонуклиарных
клеток с радиолигандом
Модель М10 прогноза
ингибирующей
активности
в отношении
15-липоксигеназы
ретикулоцитов диких кроликов
(сверхВЭС/ВЭС+СЭС+НЭС)
Ряд А – 40 структур
с высокой
ингибирующей
активностью
IC50< 0.1 мкмоль/л
Ряд В – 48 структуры
с средней ингибурующей
активностью
IC50> 0.2 мкмоль/л
Экзаменационная
выборка – 36 структур
*метод связывания
рецептора из
полиморфонуклиарных
клеток с радиолигандом
8
Типичные структуры соединений
обучающего массива
Модель М1
Модель М2
Модель М3
Модель М4
OH
F
OH
O
O
N
OH
OH
O
O
N
O
O
NH2
HO
N
O
O
Cl
O
зилеутон
N
O
O
OH
O
O
N
OH
индометоцин
O
O
NH
O
HN
N
N
OH
кетопрофен
Cl
9
Решающий набор признаков для построения модели М1
5-липоксигеназа клеток крови крыс (ВЭС/СЭС+НЭС)
№ признака
Содержимое признака
r
1
{(-O-) - (1,4-зам. бензол)}-&-{(-CH2het-) - (>N-)}-&
-{(>C=C<) -(>C=C<)}
(>N-)-&-(1,4-зам. бензол)-&-(-O-)
{(-CH2het-) - (>N-)}{(-O-) - (>C=C<)}{(>C=C<) -(>C=C<)}
(1,4-зам. бензол)-&-(-O-)-&-(>C=C<)
{(-CH2het-)-(1,4-зам. бензол)}-!-{(-N=C<)-(-O-)}-!
-{(>CH-)-((CH2)2-)}
{(-O-) - (>C=C<)}{(-CH3) - (>C<)}
{(-O-) - (>C=C<) - (>C=C<)}
(-SH)-!-(5-зам -1Н-индол)-!-(1,2-зам. бензол)
{(>CH-) - (-CH2het-) - (1-зам. бензол)}
(-NH2)-!-(5-зам -1Н-индол)-!-(1,2-зам. бензол)
{(>CH-) - (-CH2het-) - (>C=C<)}
{(-CH2het-) - (>CH-) - (-NH2)}
{(>CH-)-(>C=O)}-!-{(-OH)-(1,4-зам. бензол)}-!
-{(-CH3)-(-CH2het-)}
{(>CH-) - (-NH2)}-!-{(-OH) - (1,4-зам. бензол)}-!{(-CH3) - (-CH2het-)}
0.622
2
3
4
5
6
7
8
9
10
11
12
13
14
А=F(РНП), где
F – правила распознавания
(геометрический подход или метод
«голосования»)
0.599
0.585
0.556
0.533
0.530
0.524
-0.264
-0.278
-0.289
-0.318
-0.329
-0.381
-0.388
10
Результаты распознавания с использованием
решающего набора признаков
Метод
формирования
логических
признаков
М1
Дизъюнкции
М2
Дизъюнкции
Экзаменац
ионная
выборка
Ряд А
Ряд В
Весь массив
Экзаменац
ионная
выборка
Результат
распознаван
ия
Ряд А
Ряд В
Весь
массив
Геом.
78,57
79,59
79,08
79,54
74,19
77,94
76,07
76,23
Голос.
78,43
77,50
77,97
78,65
80,00
91,67
85,83
86,46
М3
Метод
формирования
логических
признаков
Результат
распознаван
ия
Геом.
Голос.
Дизъюнкции
Ряд А
78,49
76,34
М4
Строгие дизъюнкции
Экзаменац
ионная
выборка
Ряд А
Ряд В
Весь массив
Экзаменац
ионная
выборка
Ряд В
Весь
массив
87,80
83,15
83,24
88,24
88,89
88,56
88,35
83,93
79,64
79,57
94,12
75,00
84,56
84,49
11
Результаты распознавания с использованием
решающего набора признаков
Метод
формирования
логических
признаков
М5
М6
Дизъюнкции
Дизъюнкции
Результат
распознавания
Ряд А
Ряд В
Весь
массив
Ряд А
Ряд В
Весь
массив
Геом.
83,33
80,95
82,14
88,24
86,36
87,30
Голос.
80,56
80,95
80,75
88,24
79,55
83,89
Метод
формирования
логических
признаков
М7
М8
Строгие дизъюнкции
Строгие дизъюнкции
Результат
распознавания
Ряд А
Ряд В
Весь
массив
Ряд А
Ряд В
Весь
массив
Геом.
88,64
88,37
88,50
86,42
95,83
91,13
Голос.
86,36
88,37
87,37
88,89
72,92
80,90
12
РНП для модели М9
Метод
распозна
вания Ряд А
Геом.
Голос.
80,70
75,44
Ряд В
Весь
массив
91,30
86,00
91,30
83,37
РНП для модели М10
Экзамена
ционная
выборка
Ряд А
Экзам
Весь енацио
Ряд В масси нная
в
выбор
ка
80,56
95,50
76,09
84,29
88,90
83,33
92,50
69,57
81,03
88,90
13
Информативность
0,4
0,2
0
-0,2
0,6
0,8
1
(-CH2het-)-(-CH2het-)-(-C≡C-)
(>N-) - (>C=C<) - (-N=C<)
(-C≡C-)
(>N-)
1,2
(-CH2het-)-(-CH2het-)-(-C≡C-)
(-CH2het-) - (-N=C<) - (-S-)
(-CH3) - (>C=O) - (>C=C<)
(-CH3) - (>CH-) - (>N-)
(>N-) - (>C=C<) - (-C≡C-)
(-OH) - (>CH-) - (>C=C<)
(-N=C<) - (>C<) - (-OH)
(>SO2) - (>C=C<) - (>C=C<)
(>C<) - (>C=C<) - (>C=C<)
(>C<) - (-CH2het-) - (-O-)
(-CH3) - (>C<) - (-CH2het-)
Ациклические характерные для высоко- и среднеэффективных ингибиторов
5-липоксигеназы клеток крови человека (модели М3 и М4)
M3
M4
-0,4
Фрагменты
14
0
-0,2
-0,4
-0,6
0,6
0,4
(-CH3)
(-CH2het-)
(-CH2het-) - (>N-) - (-OH)
(>CH-) - (-O-) - (>CH-)
(>C=O) - (>C<) - (>C=C<)
(-C≡C-)
(-O-)
(Br)
0,2
Фрагменты
(-S-) - (-N=C<) - (>C=C<)
(>N-) - (>C=C<) - (>C=C<)
(-CH3) - (>C<) - (>C<)
(-CH3) - (>C<) - (>CH-)
(-N=C<)
(-NH-)
(>CH-)
(>C<)
(-CH2-)
0,8
(-CH2het-) - (>C=C<) - (>C=C<)
1
(-CH2-) - (>CH-) - (>CH-)
(-CH2het-) - (-CH2het-) - (-O-)
Информативность
Сравнительный анализ структурных дескрипторов моделей М1 и М3
(СЭС/НЭС),
где М1- модель прогноза InH 5-ЛОГ клеток крови крыс
М3 – модель прогноза InH 5-ЛОГ клеток крови человека
1,2
М1
М3
15
Влияние азот-, кислородсодержащих признаков на эффективность ингибирующего
действия по отношению к лейкотриен А4-гидролазы,
Где М5 - (ВЭС/СЭС+НЭС)
М6 - (ВЭС+СЭС/НЭС)
метод связывания рецептора из полиморфонуклиарных клеток с радиолигандом
16
Информативность, r
0
-0.2
-0.4
(-CH 3) - (-CH 2-) - (-CH 2het-)
0.2
-0.6
Фрагменты
(-CH3) - (>C=O) - (-O-)
0.4
(>CH-)
0.6
(-CH2-) - (-CH 2het-) - (>C=C<)
0.8
(-CH 2-) - (-CH2het-)
(-CH2-)
(>CH-) - (-CH 2het-) - (>C=O)
(-CH 2het-) - (>CH-) - (-CH 2het-)
(-CH 2het-) - (>CH-) - (>C=C<)
(-OH) - (>C=C<) - (>C=C<)
Ациклические признаки, характерные для
высокоэффективных антагонистов рецепторов BLT1 и BLT2
1.2
M7
1
M8
17
Ациклические признаки характерные для высокоэффективных ингибиторов
А4 гидролазы (М5) и антагонистов рецепторов BLT1 и BLT2 (М8)
18
Ациклические признаки характерные для высокоэффективных
ингибиторов
А4 гидролазы (М5) и антагонистов рецепторов BLT1 и BLT2 (М7)
19
0
-0,1
-0,2
-0,3
-0,4
Фрагменты
143
549
(-CH3) - (187)
(-CH2het-) - (549)
(-O-) - (143)
(>C=C<) - (549)
(143) - (549)
(-CH3) - (-O-) - (143)
(-CH2het-) - (143)
(>CH-) - (143)
(-NH-) - (-N=C<)
(-CH2het-) - (-CH2het-)
(-CH2het-) - (-NH-)
(-NH-) - (>C=C<)
v
(-CH2het-) - (>CH-)
(>C=C<) - (187)
(-CH2het-) - (>C=C<)
(-CH2het-) - (-(CH2)3-)
(-CH3) - (-(CH2)3-) - (-CH2het-)
(143) - (143)
0,1
(-CH2het-) - (548)
0,2
(>C=C<) - (143)
0,3
(-NH-) - (>SO2)
0,4
(>SO2) - (>C=C<)
(>SO2 ) - (143)
Информативность, r
Ациклические и циклические фрагменты, характерные для высоко( М10) и среднеэффективных (М9) ингибиторов 15-липоксигеназы
0,6
0,5
М9
М10
20
Итоговая очередность замен в нестероидных противовоспалительных
лекарственных средствах с целью конструирования эффективных
ингибиторов 5-ЛОГ, установленная по М1
3
Cl
5
O
4
CH3
O
S
O
1
5 N
O
CH 3 4
H 3CO
OH
2
O
2
1
ДВ «рефекоксиб»
ДВ «индометацин»
1
4
O
O
4
5
CH3
OH
O
O
3
ДВ «кетопрофен»
CH3 3
O
OH
2
O
3
5
1
2
ДВ «аспирин»
21
Итоговая очередность замен в эффективных ингибиторах
лейкотриен А4-гидролазы, установленная по М6
OH
2 3
5
3 2
HO
CH CH
4
1
OH2
3
5-[2-(4-гидроксифенил)винил]бензол-1,3-диол
1
1
4
S
CH2
3
5
N 2H
CH3
N-метил-1-[2-(2-тиенил)фенил]метанамин
22
Итоговая очередность замен в НПВЛС с целью конструирования эффективных
ингибиторов 15-липоксигеназы, установленная по М9
Cl
4
4
O
2
2
N
N
H3CO
O1
3
N
2
OH
3
O1
4
O1
Indometazine
Phenylbutazone
1
O
2
C
H
3
3
O
H
4
O
5
Ketoprofen
23
Структурная модификация молекулы N-метил-1-[2-(2тиенил)фенил]метанамин; r — коэффициент информативности;
пунктиром выделены модифицируемые
фрагменты молекулы и результат модификации.
r=0.112
CH3
CH3
r=-0.153
r=-0.153
r=0.355
N CH3
N CH3
S
S
CH2
CH2
NH
NH
N H
CH3
CH3
CH2
CH3
r=-0.382
r=0.112
CH3
S
CH2
N CH3
CH3
24
Высокоэффективные ингибиторы 5 - липоксигеназы
Модификация
индометацина
*
Модификация
кетопрофена
*
Модификация
аспирина
*
Модификация
рефекоксиба
*
19 80%
11 60%
Ebind=-9.4 ккал/моль
Ebind=-8.4 ккал/моль
*
*
*
*
*
14 40%
12 100%
Ebind=-7.5 ккал/моль
Ebind=-8.7 ккал/моль
*45%
*
*
25
18 90%
Ebind=-7.6 ккал/моль
Ebind=-9.3 ккал/моль
* - структуры с прогнозируемой высокой противовоспалительной активностью в отношении изоформ ЦОГ
25
Высокоэффективные ингибиторы лейкотриен А4-гидролазы
полученные в результате модификации
Модификация 5-[2-(4гидроксифенил)винил]бензол-1,3-диол
*
*
O
OH
HO
Модификация N-метил-1-[2-(2тиенил)фенил]метанамин
*
*
*
*
*
*
HO
N
OH
*
*
O
HO
O
HO
N
HO
OH
*
CN
H
O
*
O
OH
* - структуры с высокой противовоспалительной активностью
O
26
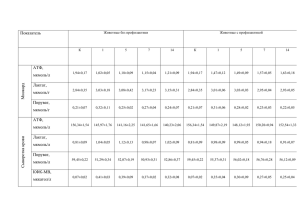
Результаты гибкого докинга лигандов R11, R12, R18 в активный центр фермента 5-ЛОГ,
выполненного с использованием программы AutoDock 4.2
(в качестве модели макромолекулы выбрана макромолекула с кодом 3о8у (PDB))
qstep=30, tstep=30
Коньюгаты бетулоновой и бетулиновой кислот с амидными производными
кислоты Тролокс.
OH
H
N
H
N
O
O
O
O
предсказано
O
H
H
N
H
N
O
O
O
HO
27
Выводы по моделированию ингибиторов 5-ЛОГ
1. Выявлены структурные признаки характерные для высокоэффективных и
среднеэффективных ингибиторов активности 5-липоксигеназы.
2. Построены 4 модели прогноза и распознавания М1,М2, М3 и М4 отличающиеся
интервальным уровнем прогноза и распознавания ингибирующей активности
различных классов соединений в отношении 5-липоксигеназы с уровнем
достоверного прогноза выше 76 % по двум методам теории распознавания образов.
3. Построены 2 модели прогноза и распознавания М5 и М6, отличающиеся
интервальным уровнем прогноза и распознавания ингибирующей активности
различных классов соединений в отношении лейкотриен А4-гидролазы с уровнем
достоверного прогноза выше 80 % по двум методам теории распознавания образов.
4. Построены 2 модели прогноза и распознавания (М7 и М8) эффективных блокаторов
рецепторов BLT1 и BLT2, чувствительных к лейкотриенам, с уровнем достоверного
прогноза выше 80 % по двум методам теории распознавания образов.
5. В результате структурной модификации действующих веществ ―аспирин‖,
―кетопрофен‖, ―индометоцин‖ и ―рефококсиб‖ получено 92 потенциально
высокоактивных ингибиторов 5-липоксигеназы, и 72 из них обладают выраженной
противовоспалительной активностью
28
6. В результате структурной модификации 5-[2-(4гидроксифенил)винил]бензол-1,3-диола и N-метил-1-[2-(2тиенил)фенил]метанамина получено 54 потенциально
высокоактивных ингибитора активности лейкотриен А4-гидролазы.
7. Предсказано, что ранее неизвестные в качестве лекарственных
препаратов коньюгаты бетулинвой и бетулоновой кислот м амидным
производным кислоты Тролокс должны обладать
противовоспалительной активностью. Согласно результатам
фармокологических испытаний эти вещества обладает ярко
выраженной противовоспалительной активностью. И могут быть
рекомендованы для дальнейшего изучения в целях возможного
получения нового противовоспалительного препарата.
29
QSAR-study 15-LOX inhibitors with MOE (Germany, Halle)
1. Selection of training set of 15-LOX inhibitors using MCS (Marvin).
2. Revealing of the effect of QSAR-descriptors on the manifestation of the
activity type studied.
3. Construction of a mathematical modelies for 15-LOX inhibitory
activity prediction.
4. Test of the QSAR-model by cross-validation.
5. Prediction of activity by using the derived multilinear regression for
some new structures
A series of inhibitors of mammalian 15-LOX based on tryptamine,
homotryptamine scaffolds and iminazole is using QSAR methodology
studied. Its activity interval has been at 0,006 — 10 mkMol/l. Compounds
with aryl substituents at C2 of the indole core of tryptamine and
homotryptamine sulfonamides proved to be potent inhibitors of the
isolated enzyme.
30
QSAR-Untersuchung von Indolderivatives zur inhibierenden Aktivität gegen der 15-LOX
(Weinstein, 2005)
l
g
1
/
I
C
7
.
8
4
8
0
.
0
6
8
•
v
s
a
_
d
o
n
0
.
3
6
6
•
l
o
g
P
(
o
/
w
)
3
.
8
6
1
•
g
l
o
b
0
.
0
8
9
•
o
p
r
_
b
r
i
g
i
d
5
0
2
2
n
4
6
,
r
0
.
8
1
,
s
0
.
4
2
7
,
q
0
.
7
8
,
q
s
0
.
4
7
5Eq1
l
g
1
/
I
C
8
.
1
1
1
0
.
5
5
6
•
l
o
g
P
(
o
/
w
)
2
.
8
0
3
•
g
l
o
b
0
.
2
3
2
•
l
i
p
_
a
c
c
0
.
5
5
5
•
F
C
A
S
A
5
0
2
2
n
4
6
,
r
0
.
8
2
,
s
0
.
4
1
6
,
q
0
.
7
8
,
q
s
0
.
4
5
7
Eq2
lg 1/ IC 52.180 0.417•log P(o / w) 67.702•GCUT _ PEOE _00.026• PEOE _ VSA_2 0.487• adon
50
2
2
n
4
6
,
r
0
.
8
5
,
s
0
.
4
1
6
,
q
0
.
7
8
,
q
s
0
.
4
5
7
Eq3
l
g
1
/
I
C
4
0
.
0
3
7
0
.
4
6
5
•
l
o
g
P
(
o
/
w
)
0
.
2
5
0
•
l
i
p
_
a
c
c
5
4
.
1
5
7
G
C
U
T
P
E
O
E
0
5
0
Eq4
n 46, r 2 0.84, s 0.394, q 2 0.78, qs 0.460
31
l
g
1
/
I
C
6
.
4
0
3
0
.
3
1
9
•
S
M
R
2
.
4
9
8
•
g
l
o
b
0
.
0
6
0
•
E
0
.
3
6
2
•
a
d
o
n
s
o
l
5
0
2
2
Eq5
n
4
6
,
r
0
.
8
2
,
s
0
.
4
1
4
,
q
0
.
7
8
,
q
s
0
.
4
6
4
l
g
1
/
I
C
5
.
6
0
1
0
.
0
4
4
•
E
0
.
4
9
4
•
S
M
R
0
.
0
1
4
•
P
E
O
E
_
V
S
A
0
0
.
9
3
6
•
A
M
1
_
L
U
M
O
s
o
l
5
0
2
2
n
4
6
,
r
0
.
8
4
,
s
0
.
3
9
8
,
q
0
.
7
9
,
q
s
0
.
4
5
6
Eq6
lg 1/ IC 5.702 0,052• E 0.419• SMR 0.009• PEOE _VSA 0
50
sol
n 46, r 2 0.82, s 0.420, q 2 0.78, qs 0.460
Eq7
With these QSAR-equations we have generated activity date for new structures
predicted from SARD (Fig. 1).
32
l
g
1
/
I
C
4
0
.
0
3
7
0
.
4
6
5
•
l
o
g
P
(
o
/
w
)
0
.
2
5
0
•
l
i
p
_
a
c
c
5
4
.
1
5
7
G
C
U
T
P
E
O
E
0
5
0
Eq4
n 46, r 2 0.84, s 0.394, q 2 0.78, qs 0.460
33
lg 1/ IC 5.702 0,052• E 0.419• SMR 0.009• PEOE _VSA 0
50
sol
n 46, r 2 0.82, s 0.420, q 2 0.78, qs 0.460
Eq7
34
Потенциально эффективные ингибиторы 15-ЛОГ, полученные в
результате молекулярного дизайна ДВ НПВЛС «Индометацин»
Cl
O
O
C
H
3
Cl
O
O
N
N
N
H3CO
NH
OH
O
H3CO
S O
NH
O
S
H
O
3C
S
O O
O
HO
1
208 1 нмоль/ла
193 1 нмоль/лб
2
99 1 нмоль/ла
52 1 нмоль/лб
Cl
O
Cl
O
N
3
222 1 нмоль/ла
16 1 нмоль/лб
C
l
O
N
N
H
O
3C
H3CO
S CF
3
S
4
127 1 нмоль/ла
31 1 нмоль/лб
H3CO
S
5
2594 1 нмоль/ла
559 1 нмоль/лб
Cl
O
S
S NH
2
S
N
H
O
C
H
3
6
620 1 нмоль/ла
209 1 нмоль/лб
O
C
H
3
Cl
O
O
N
N
H3CO
S
N
S
7
364 1 нмоль/ла
28 1 нмоль/лб
H
O
3C
H
O
3C
H
S S O
8
342 1 нмоль/ла
114 1 нмоль/лб
N
H
S
O
C
H
3
O O
9
282 1 нмоль/ла
61 1 нмоль/лб
а – расчет значений IC50 выполнен по линейному регрессионному уравнению (4);
б – расчет значений IC50 выполнен по линейному регрессионному уравнению (7).
35
QSAR-Untersuchung von Imidazolderivatives zur inhibierenden Aktivität
gegen der 15-LOX
(Weinstein, 2007)
l
g
1
/
I
C
2
.
2
3
1
0
.
1
7
3
•
S
M
R
_
V
S
A
3
0
.
2
9
4
•
l
o
g
S
0
.
0
8
2
•
P
E
O
E
_
V
S
A
_
2
0
.
6
9
3
•
d
i
p
o
l
e
Y
5
0
2
2
Eq1
n
2
2
,
r
0
.
8
0
,
s
0
.
4
3
0
,
q
0
.
6
0
4
,
q
s
0
.
6
2
2
lg 1/ IC50 13.640 0.197• SMR_ VSA3 0.088• PEOE _ VSA_2
0.352•log S 0.841• dipoleY 23.086• petitjean
Eq2
2
2
n
2
2
,
r
0
.
8
5
,
s
0
.
3
7
0
,
q
0
.
6
9
4
,
q
s
0
.
5
4
0
l
g
1
/
I
C
7
.
2
9
2
0
.
2
7
9
•
c
h
i
v
0
0
.
0
1
3
2
9
•
A
M
1
_
H
F
v
0
5
Eq3
0
.
0
0
4
•
S
L
o
g
P
_
V
S
A
3
0
.
0
2
5
•
v
s
a
_
d
o
n
2
2
n
1
6
,
r
0
.
8
0
,
s
0
.
2
4
4
,
q
0
.
5
6
4
,
q
s
0
.
3
7
2
36
lg 1/ IC50 13.640 0.197• SMR_ VSA3 0.088• PEOE _ VSA_2
Eq2
0.352•log S 0.841• dipoleY 23.086• petitjean
2
2
n
2
2
,
r
0
.
8
5
,
s
0
.
3
7
0
,
q
0
.
6
9
4
,
q
s
0
.
5
4
0
37
Potentially high effective generated structures on the indometazin and
Phenylbutazone structures base estimated using DAS for M2
and QSAR-equation 2 for Imidazolderivates.
Auf Grund von Indometazin
O
C
H
3
N
H
N
O
S N
H
2
O
IC50=0,53 nM
Auf Grund von Phenylbutazone
OCH3
O
OCH3
N
H
O
S
N
N
HS
O
NH
O
N
N
H3CO
NH
OCH3
IC50=14250 nM
N
H
N
O
C
H
3
N
H
O
C
H
3
H
C
O
3
IC50=3162 nM
IC50=3550 nM
IC50=3890 nM
38
Выводы
•
Выявлены структурные признаки, характерные для эффективных и
высокоэффективных ингибиторов 15-липоксигеназы.
•
Построены две модели прогноза интервальных уровней ингибирующей
активности серу- азот- и кислородсодержащих гетероциклических соединений
на фермент 15-липоксигеназы с уровнем достоверного прогноза 80 % по двум
методам теории распознавания образов.
•
Установлено, что определяющий положительный вклад в проявление
ингибирующей активности ряда сульфонамидов незамещенных, С-2 и 2-(2бензофуранилзамещенных триптаминов и гомотриптаминов оказывают
поляризуемость этих молекул и их энергия сольватации.
•
Построены 10 линейных регрессионных модели прогноза ингибирующей
активности для ряда сульфонамидов незамещенных, С-2 и 2-(2бензофуранилзамещенных триптаминов и гомотриптаминов.
•
В результате молекулярного дизайна [1-(4-хлорбензол)-5-метокси-2метил-1Н-индол-3-ил] уксусной кислоты (действующее вещество НПВЛС
«индометацин») получено 33 потенциально высоко- и и среднеэффективных
ингибиторов 15-ЛОГ. Активность этих соединений количественно
охарактеризована значениями IC50, оцененными по линейно-регрессионным
моделям.
39
Спасибо за внимание!!!