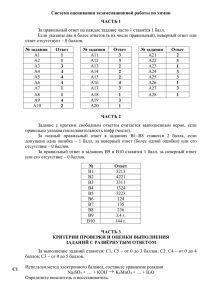
Используя метод электронного баланса, составьте уравнение реакции: → CO HCOH + KMnO
реклама

Критерии оценивания выполнения заданий с развернутым ответом Единый государственный экзамен, 2008 г. ХИМИЯ, 11 класс. C1 Вариант: 5 Единый государственный экзамен, 2008 г. (стр 1 / 4) Ответ: Баллы (допускаются иные формулировки ответа, не искажающие его смысла) C3 2) Расставлены все коэффициенты в уравнении реакции: 5HCOH + 4KMnO4 + 6H2SO4 = 5CO2 + 2K2SO4 + 4MnSO4 + 11H2O Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: 2+ + H2 O (H ) → X3 → уксусная кислота. 3 2 1 0 3 Даны вещества: оксид натрия, оксид железа (III), иодоводород и углекислый газ. Напишите уравнения четырех возможных реакций между этими веществами. Ответ: Ответ: Содержание верного ответа и указания по оцениванию Элементы ответа: Написаны четыре уравнения возможных реакций между указанными веществами: 1) Na2O + Fe2O3 = 2NaFeO2 2) 2HI + Na2O = 2NaI + H2O 3) Na2O + CO2 = Na2CO3 4) Fe2O3 + 6HI = 2FeI2 + I2 + 3H2O © 2008 Федеральная служба по надзору в сфере образования и науки Российской Федерации Копирование не допускается Баллы Баллы (допускаются иные формулировки ответа, не искажающие его смысла) Элементы ответа: Написаны уравнения реакций, соответствующие схеме превращений: 1) HC 2) 5H3C 3) H3C 4) H3C Содержание верного ответа и указания по оцениванию + H2 O (Hg ) KMnO4 , H NaOH CH3I HC ≡ CH → X1 → CH3COOH → X2 → 3) Указано, что углерод в степени окисления 0 (или формальдегид за счет углерода) является восстановителем, а марганец +7 (или перманганат калия за счет марганца +7) – окислителем. Ответ правильный и полный, включает все названные выше элементы В ответе допущена ошибка только в одном из элементов В ответе допущены ошибки в двух элементах Все элементы ответа записаны неверно Максимальный балл (допускаются иные формулировки ответа, не искажающие его смысла) 4 3 2 1 0 4 *Примечание. Дополнительно записанные (правильно или ошибочно) уравнения реакций не оцениваются. Элементы ответа: 1) Составлен электронный баланс: 5 C0 – 4ē → C+4 4 Mn+7 + 5ē → Mn+2 C2 (стр 2 / 4) Правильно записаны 4 уравнения возможных реакций Правильно записаны 3 уравнения реакций Правильно записаны 2 уравнения реакций Правильно записано 1 уравнение реакции Все элементы ответа записаны неверно Максимальный балл Используя метод электронного баланса, составьте уравнение реакции: HCOH + KMnO4 + ... → CO2 + K2SO4 + ... + … . Укажите окислитель и восстановитель. Содержание верного ответа и указания по оцениванию ХИМИЯ, 11 класс. 5) H3C CH + H2O Hg2+ H3C C O H O + 2KMnO4 + 3H2SO4 H O H 3C + NaOH C OH O H 3C + CH3I C ONa + H O + H2O H3C C OCH3 C 5 H3C C O + 2MnSO4 + K2SO4 + 3H2O OH O + H2O ONa O + NaI C OCH3 C C O + CH3OH OH Ответ правильный и полный, включает все названные выше элементы Правильно записаны 4 уравнения реакций Правильно записаны 3 уравнения реакций Правильно записаны 2 уравнения реакций Правильно записано 1 уравнение реакции Все элементы ответа записаны неверно Максимальный балл 5 4 3 2 1 0 5 Критерии оценивания выполнения заданий с развернутым ответом Единый государственный экзамен, 2008 г. ХИМИЯ, 11 класс. C4 Вариант: 5 Единый государственный экзамен, 2008 г. (стр 3 / 4) Какой объем 30%-ного раствора аммиака (ρ = 0,892 г/мл) необходимо добавить к 200 мл 40%-ного раствора соляной кислоты (ρ = 1,198 г/мл), чтобы массовая доля кислоты уменьшилась вчетверо? C5 ХИМИЯ, 11 класс. (стр 4 / 4) При взаимодействии 30 г предельного одноатомного спирта с металлическим натрием выделилось 5,6 л (н.у.) газа. Определите молекулярную формулу спирта. Ответ: Ответ: Содержание верного ответа и указания по оцениванию Баллы (допускаются иные формулировки ответа, не искажающие его смысла) 2) Рассчитаны массы веществ, вступивших в реакцию: Vр-ра(NH3) = x мл, m(NH3) = Vр-ра(NH3) · w(NH3) · ρ(NH3) = x·0,3·0,892 = 0,2676x mисх(HCl) = Vр-ра(HCl) · ρ(HCl) · w(HCl) = 200·0,4·1,198 = 95,84 г mпрореагир.(HCl) = M(HCl)·m(NH3)/M(NH3) = 36,5·0,2676x/17 = 0,575x 2) Рассчитана молярная масса спирта: n(СnH2n+1OH) = 2n(Н2) = 0,5 моль М(СnH2n+1OH) = 30/0,5 = 60 г/моль 3) Установлена молекулярная формула спирта: М(СnH2n+1COOH) = 12n + 2n + 1 + 17 = 60 14n + 18 = 60 14n = 42 n=3 Молекулярная формула спирта C3H7OH 3) Рассчитана масса оставшегося хлороводорода и масса раствора mизб(HCl) = mисх.(HCl) − mпрореагир.(HCl) = 95,84 − 0,575x m(раствора) = mр-ра (HCl) + mр-ра (NH3) = 200·1,198 + 0,892x = = 239,6 + 0,892x © 2008 Федеральная служба по надзору в сфере образования и науки Российской Федерации Копирование не допускается Баллы Элементы ответа: 1) Составлено уравнение реакции в общем виде, и вычислено количество вещества газа: 2СnH2n+1OH + 2Na = 2СnH2n+1CONa + H2 n(Н2) = 0,25 моль Элементы ответа: 1) Составлено уравнение химической реакции: NH3 + HCl = NH4Cl 4) Найден объем раствора аммиака: w(HCl)= mизб.(HCl)/m(раствора) 0,1 = (95,84−0,575x)/(239,6 + 0,892x) откуда x = 108,2 мл. Ответ правильный и полный, включает все названные выше элементы В ответе допущена ошибка в одном из названных выше элементов В ответе допущена ошибка в двух из названных выше элементов В ответе допущена ошибка в трех из названных выше элементов Все элементы ответа записаны неверно Максимальный балл Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) 4 3 2 1 0 4 Ответ правильный и полный, включает все названные выше элементы Правильно записаны первый и второй элементы ответа Правильно записан первый или второй элементы ответа Все элементы ответа записаны неверно Максимальный балл 3 2 1 0 3